题目内容
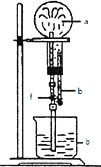 在图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
在图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )| A、NO和H2O |
| B、Cl2和饱和食盐水 |
| C、NH3和水 |
| D、NO2和H2O |
考点:实验装置综合,氯气的化学性质,氨的化学性质,氮的氧化物的性质及其对环境的影响
专题:元素及其化合物
分析:此题要从反应物和生成物的状态变化入手,注意到反应后气体减少或增多会引起气压的变化,则气体被吸收进溶液的反应,容器内气体减少,气压减小,a中的气体极易被b中试剂吸收或发生化学反应导致气压减小,以此来解答.
解答:
解:A.一氧化氮和水不反应,所以不能形成喷泉实验,故A错误;
B.Cl2不溶于饱和氯化钠溶液,也不与其反应,锥形瓶与烧瓶内压强相等,不能形成喷泉,故B错误;
C.NH3易溶于水,气体被吸收进溶液中,烧瓶内压强减小为零,同外界大气压产生压强差,所以形成喷泉,并充满烧瓶,故C正确;
D.NO2与水反应,生成硝酸和NO,容器内气体减少,气压减小,形成喷泉,但由于NO不溶于水,所以不充满烧瓶.故D错误.
故选C.
B.Cl2不溶于饱和氯化钠溶液,也不与其反应,锥形瓶与烧瓶内压强相等,不能形成喷泉,故B错误;
C.NH3易溶于水,气体被吸收进溶液中,烧瓶内压强减小为零,同外界大气压产生压强差,所以形成喷泉,并充满烧瓶,故C正确;
D.NO2与水反应,生成硝酸和NO,容器内气体减少,气压减小,形成喷泉,但由于NO不溶于水,所以不充满烧瓶.故D错误.
故选C.
点评:本题考查喷泉实验,注意反应物或生成物的状态变化会引起气压的变化,把握化学和物理的联系,知道解决化学问题可以应用物理知识,题目难度不大.

练习册系列答案
相关题目
下列说法中错误的是( )
| A、化学反应中的能量变化通常表现为热量的变化 |
| B、化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C、反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
| D、需要加热才能发生的化学反应一定是吸热反应 |
已知25℃,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36.常温时下列有关说法正确的是( )
| A、除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
| B、将足量CuSO4溶解在0.1mol?L-1 H2S溶液中,Cu2+的最大浓度为1.3×10-35mol?L-1 |
| C、因为H2SO4是强酸,所以反应CuSO4+H2S═CuS↓+H2SO4不能发生 |
| D、向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强 |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等七种离子中的几种.现取该溶液进行实验,有如下实验现象:据此可以推断,该溶液中肯定不存在的离子是( )
①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生
②向所得橙色溶液中滴加足量BaCl2溶液,无沉淀生成
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生
②向所得橙色溶液中滴加足量BaCl2溶液,无沉淀生成
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
| A、Mg2+、Na+、CO32-、I- |
| B、Al3+、Na+、SO32-、I- |
| C、Al3+、Mg2+、SO32-、I- |
| D、Al3+、CO32-、Br-、SO32- |
氮化钠(Na3N)熔融时能导电,与水作用产生NH3.下列对氮化钠晶体描述错误的是( )
| A、构成晶体的两种微粒电子层结构相同 |
| B、构成晶体的两种微粒半径不相等 |
| C、与盐酸反应生成盐的化学键类型相同 |
| D、与盐酸反应生成盐的晶体类型相同 |
设NA为阿伏加德罗常数的值.下列说法不正确的是( )
| A、由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
| B、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.2NA |
| D、2mol SO2和1mol O2在一定条件下充分反应后,所得混合气体的分子数小于2NA |
某有机化合物的结构简式为 它可以发生的反应类型有( )
它可以发生的反应类型有( )
a取代 b加成 c消去 d酯化 e水解 f中和 g缩聚 h加聚.
 它可以发生的反应类型有( )
它可以发生的反应类型有( )a取代 b加成 c消去 d酯化 e水解 f中和 g缩聚 h加聚.
| A、acdf | B、befh |
| C、abcd | D、除eh外 |
2HCHO+NaOH(浓)→CH3OH+HCOONa,该反应中甲醛发生的反应类型是( )
| A、仅被氧化 |
| B、仅被还原 |
| C、既被氧化又被还原 |
| D、复分解反应 |