题目内容
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等七种离子中的几种.现取该溶液进行实验,有如下实验现象:据此可以推断,该溶液中肯定不存在的离子是( )
①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生
②向所得橙色溶液中滴加足量BaCl2溶液,无沉淀生成
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生
②向所得橙色溶液中滴加足量BaCl2溶液,无沉淀生成
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
| A、Mg2+、Na+、CO32-、I- |
| B、Al3+、Na+、SO32-、I- |
| C、Al3+、Mg2+、SO32-、I- |
| D、Al3+、CO32-、Br-、SO32- |
考点:常见离子的检验方法,离子共存问题
专题:离子反应专题
分析:①向溶液中滴加足量氯水后,溶液变橙色,说明溶液中含有Br-,且有无色气泡冒出,说明溶液中含离子CO32-;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成,说明不含SO32-;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色,说明溶液中不含I-,据此进行解答.
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成,说明不含SO32-;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色,说明溶液中不含I-,据此进行解答.
解答:
解:根据①可知溶液中含有Br-,有无色气泡冒出,说明溶液中含离子CO32-,则一定不含有Al3+、Mg2+,因与CO32-反应生成沉淀;
根据②可知,溶液中一定不含SO32-;
根据③液不变蓝色,说明溶液中不含I-;
据溶液呈电中性原则,溶液中一定含有Na+,
所以溶液中一定不存在的离子为:Al3+、Mg2+、I-、SO32-,一定含有的离子为:CO32-、Br-、Na+,
故选C.
根据②可知,溶液中一定不含SO32-;
根据③液不变蓝色,说明溶液中不含I-;
据溶液呈电中性原则,溶液中一定含有Na+,
所以溶液中一定不存在的离子为:Al3+、Mg2+、I-、SO32-,一定含有的离子为:CO32-、Br-、Na+,
故选C.
点评:本题考查离子的检验及离子共存问题,题目难度中等,注意掌握常见离子的性质及检验方法,明确常见离子的反应的现象,然后结合离子的性质进行判断.

练习册系列答案
相关题目
可用如图装置制取(必要时可加热、尾气处理已省略)、净化、收集的气体是( )


| A、氯化钠固体与浓硫酸制氯化氢 |
| B、铜和稀硝酸制一氧化氮 |
| C、锌和稀硫酸制氢气 |
| D、用生石灰和浓氨水制氨气 |
 A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )| A、简单离子的半径大小关系:B>C>E |
| B、D元素的气态氢化物比C元素的气态氢化物稳定 |
| C、由A、B、C三种元素组成的离子化合物NH4NO3中,阴、阳离子个数比为1:1 |
| D、由C、D、E三种元素组成的某种化合物,水解显碱性 |
下列元素中属于短周期元素的是( )
| A、碘 | B、铁 | C、钙 | D、氩 |
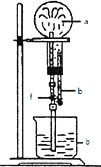 在图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
在图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )| A、NO和H2O |
| B、Cl2和饱和食盐水 |
| C、NH3和水 |
| D、NO2和H2O |
Fe3+、SO42-、Al3+和X四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,则X可能是( )
| A、Na+ |
| B、Cl- |
| C、CO32- |
| D、OH- |
短周期元素X、Y、Z的原子序数依次增大,Y为IA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13.下列判断正确的是 ( )
| A、Y元素位于第2周期 |
| B、Y、Z均能与X形成不只一种化合物 |
| C、X是ⅤA族元素 |
| D、氢化物的稳定性:HnZ>HnX |
化学是一门以实验为基础的自然科学,下列实验中所选用的仪器不合理的是( )
| A、用分液漏斗分离苯和乙醇的混合物 |
| B、用托盘天平称量11.7g氯化钠晶体 |
| C、用25mL滴定管量取23.10mL Na2CO3溶液 |
| D、用500mL容量瓶配制所需490mL 0.1mol/L的NaCl溶液 |