题目内容
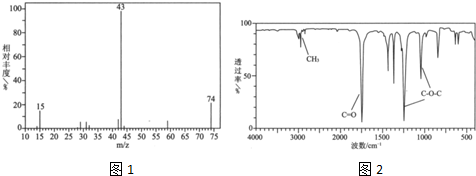
 如图,在密闭容器中反应:C(s)+H2O(g)?CO(g)+H2(g) (吸热反应)达到平衡后,由于条件的改变而引起正、逆反应速率的变化,及平衡移动状况,则改变的条件是( )
如图,在密闭容器中反应:C(s)+H2O(g)?CO(g)+H2(g) (吸热反应)达到平衡后,由于条件的改变而引起正、逆反应速率的变化,及平衡移动状况,则改变的条件是( )| A、增加CO浓度 | B、增大压强 |
| C、升高温度 | D、增加水蒸气 |
考点:化学反应速率变化曲线及其应用
专题:化学平衡专题
分析:根据正逆反应速率的变化结合温度、压强对反应速率和化学平衡的影响判断,a时逆反应速率大于正反应速率,且正逆反应速率都增大,b时正反应速率大于逆反应速率,注意逆反应速率突然减小的特点,据此进行解答.
解答:
解:根据图可知,在条件改变时正逆反应速率都增大,可能为增大压强或者升高温度,且逆反应速率大于正反应速率,平衡向着逆向移动,若最大压强,平衡向着逆向移动,逆反应速率大于正反应速率,满足条件;该反应的正反应吸热反应,若升高温度后平衡向着正向移动,正反应速率大于逆反应速率,所以不可能为升高温度,应该为增大压强;
故选B.
故选B.
点评:本题考查化学反应速率与化学平衡图象的综合应用,题目难度不大,注意把握曲线的变化趋势以及外界条件对化学平衡的影响,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
已知NH3极易溶于水,下列组合中不能形成喷泉的是( )
| A、HCl和H2O |
| B、O2和H2O |
| C、NH3和H2O |
| D、CO2和NaOH |
下列说法正确的是( )
| A、丙烷是直链烃,所以分子中3个碳原子也在一条直线上 |
| B、丙烯所有原子均在同一平面上 |
C、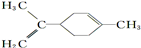 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D、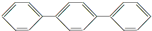 至少有16个原子共平面 至少有16个原子共平面 |
氯化溴(BrCl)和Br2、Cl2具有相似的性质,下列有关氯化溴性质的判断中错误的是( )
| A、在CCl4中的溶解性BrCl<Br2 |
| B、BrCl氧化性比Br2强,比Cl2弱 |
| C、沸点BrCl>Br2 |
| D、常温下BrCl可与NaOH溶液反应生成NaCl和NaBrO |
用NA表示阿伏加德罗常数的值,下列叙述错误的是( )
| A、含有NA个氢原子的氢气在标准状况下的体积约为11.2L |
| B、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| C、在常温常压下,35.5g Cl2含有的分子数为0.5NA |
| D、标准状况下,11.2L H2O含有的分子数为0.5NA |