题目内容
5.未污染的雨水由于二氧化碳的缘故,一般呈现出弱酸性,当雨水的pH<5.6时,我们称之为“酸雨”.酸雨露置于空气中,经过一段时间后中,pH值会变小(填“变大”、“变小”或“不变”).控制酸雨的措施有acda.使用脱硫煤
b.加高工厂的烟囱
c.用废碱液吸收烟气中的二氧化硫
d.开发新能源.
分析 正常雨水中溶解二氧化碳,为弱酸性,而溶解二氧化硫的雨水的酸性增强,pH<5.6,亚硫酸与氧气反应生成硫酸,酸性增强,pH变小,可控制二氧化硫的排放,减少酸雨的发生,以此来解答.
解答 解:未污染的雨水由于二氧化碳的缘故,一般呈现出弱酸性,当雨水的pH<5.6时,我们称之为“酸雨”.酸雨露置于空气中,经过一段时间后中,亚硫酸与氧气反应生成硫酸,酸性增强,pH值会变小;控制酸雨的措施有a.使用脱硫煤、c.用废碱液吸收烟气中的二氧化硫、d.开发新能源,均可减少二氧化硫的排放,只有b.加高工厂的烟囱不能减少二氧化硫的排放,
故答案为:二氧化碳;<;变小;acd.
点评 本题考查三废处理及环境保护,为高频考点,把握酸雨的形成、控制酸雨的措施为解答的关键,侧重分析与应用能力的考查,注意化学与环境的联系,题目难度不大.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
20.化学键的键能是指气态基态原子间形成1mol 化学键时释放的最低能量.如:H(g)+I(g)-→H-I(g)+297kJ,即H-I键的键能为297kJ/mol,也可以理解为破坏1mol H-I键需要吸收297kJ的热量.化学反应的发生可以看成旧化学键的破坏和新化学键的形成.
表是一些键能数据(单位:kJ/mol):
阅读上述信息,回答下列问题:
(1)根据表中数据判断CCl4的稳定性小于(填“大于”或“小于”)CF4的稳定性.试预测C-Br键的键能范围:218 kJ/mol<C-Br键键能<330 kJ/mol.
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)═2HCl(g)△H=-Q kJ/mol,则热化学方程式中Q的值为185.
(3)由表中数据能否得出这样的结论:
①半径越小的原子形成的共价键越牢固(即键能越大).不能(填“能”或“不能”).
②非金属性越强的原子形成的共价键越牢固.不能(填“能”或“不能”).从数据中找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强.
表是一些键能数据(单位:kJ/mol):
| 键能 | 键能 | 键能 | |||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | ||
| S-S | 255 | H-S | 339 | C-F | 427 | ||
| C-Cl | 330 | C-I | 218 | H-F | 568 | ||
| C-O | 351 | H-O | 463 |
(1)根据表中数据判断CCl4的稳定性小于(填“大于”或“小于”)CF4的稳定性.试预测C-Br键的键能范围:218 kJ/mol<C-Br键键能<330 kJ/mol.
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)═2HCl(g)△H=-Q kJ/mol,则热化学方程式中Q的值为185.
(3)由表中数据能否得出这样的结论:
①半径越小的原子形成的共价键越牢固(即键能越大).不能(填“能”或“不能”).
②非金属性越强的原子形成的共价键越牢固.不能(填“能”或“不能”).从数据中找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强.
1.下列说法不正确的是( )
| A. | 物质所含元素化合价升高的反应是氧化反应 | |
| B. | 物质所含元素化合价降低的反应是还原反应 | |
| C. | 氧化剂本身被还原,具有氧化性;还原剂本身被氧化,具有还原性 | |
| D. | 氧化反应和还原反应不一定同时存在于一个反应中 |
17.氨气是重要的化工原料已知:
N2(g)+O2(g)=2NO(g)△H=+akJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-bkJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-ckJ•mol-1
则N2(g)+3H2(g)?2NH3(g)的反应热△H为( )
N2(g)+O2(g)=2NO(g)△H=+akJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-bkJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-ckJ•mol-1
则N2(g)+3H2(g)?2NH3(g)的反应热△H为( )
| A. | (a+0.5b-1.5c) kJ•mol-1 | B. | (a-0.5b+1.5c) kJ•mol-1 | ||
| C. | (2a+b-3c) kJ•mol-1 | D. | (2a+b+3c) kJ•mol-1 |
14.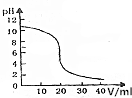 常温下,向20mL0.1000mol•L-1的氨水溶液中逐滴加入0.1000mol•L-的盐酸,pH随盐酸体积的变化如图所示.下列说法不正确的是( )
常温下,向20mL0.1000mol•L-1的氨水溶液中逐滴加入0.1000mol•L-的盐酸,pH随盐酸体积的变化如图所示.下列说法不正确的是( )
 常温下,向20mL0.1000mol•L-1的氨水溶液中逐滴加入0.1000mol•L-的盐酸,pH随盐酸体积的变化如图所示.下列说法不正确的是( )
常温下,向20mL0.1000mol•L-1的氨水溶液中逐滴加入0.1000mol•L-的盐酸,pH随盐酸体积的变化如图所示.下列说法不正确的是( )| A. | V=10.00mL时,c(NH4+)+c(NH3•H2O)=2c(Cl-) | |
| B. | V=20.00mL时,c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | pH=7时,消耗盐酸的体积大于20.00mL | |
| D. | pH=8时,c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
15.人类只有一个地球,保护环境、保护地球已成为人类共同的呼声.下列说法不正确的是( )
| A. | 日本的水俣病是由重金属镉污染引起的 | |
| B. | 垃圾处理要遵循无害化、减量化和资源化的原则 | |
| C. | 水体的富营养化是由于水体中植物营养物质过多蓄积而引起的污染 | |
| D. | 污水处理中混凝法、中和法、沉淀法、氧化还原法等都是化学方法 |
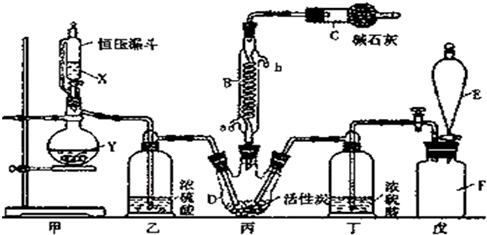
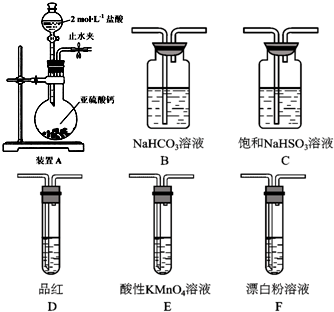
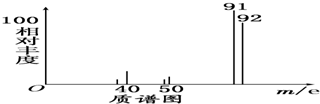
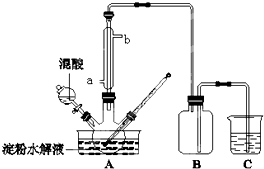 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下: