题目内容
1.下列说法不正确的是( )| A. | 物质所含元素化合价升高的反应是氧化反应 | |
| B. | 物质所含元素化合价降低的反应是还原反应 | |
| C. | 氧化剂本身被还原,具有氧化性;还原剂本身被氧化,具有还原性 | |
| D. | 氧化反应和还原反应不一定同时存在于一个反应中 |
分析 氧化还原反应的实质为电子转移,其特征为化合价的变化,氧化还原反应中不一定有氧元素或单质参加和生成,以此来解答.
解答 解:A.物质所含元素化合价升高的反应,失去电子,被氧化,发生氧化反应,故A正确;
B.物质所含元素化合价降低的反应,得电子,被还原,是还原反应,故B正确;
C.氧化剂化合价降低,得电子被还原,具有氧化性,还原剂失电子,化合价升高,被氧化,具有还原性,故C正确;
D.氧化还原反应中有氧化反应,也一定有还原反应,即氧化反应和还原反应一定同时存在于一个反应中,故D错误;
故选D.
点评 本题考查氧化还原反应,把握基本概念及常见的实例为解答的关键,侧重氧化还原反应实质和特征的考查,题目难度不大.

练习册系列答案
相关题目
11.常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①、②、③的实验,实验数据记录如下表
请回答:
(1)根据①组实验情况,分析混合溶液的pH=9的原因是H2O+A-?HA+OH-.(用反应的离子方程式表示),在该溶液中下列关系式正确的是(填序号字母)BD.
A.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA) B.c(Na+)=c(HA)+c(A-)
C.c(HA)+c(H+)=c(OH-)+c(Na+) D.c(Na+)+c(H+)=c(OH-)+c(A-)
(2)②组情况表明,c>0.2mol•L-1(选填“>”、“<”或“=”).混合溶液中离子浓度c(A-)=c(Na+)(选填“>”、“<”或“=”)
(3)从③组实验结果分析,说明溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)根据①组实验情况,分析混合溶液的pH=9的原因是H2O+A-?HA+OH-.(用反应的离子方程式表示),在该溶液中下列关系式正确的是(填序号字母)BD.
A.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA) B.c(Na+)=c(HA)+c(A-)
C.c(HA)+c(H+)=c(OH-)+c(Na+) D.c(Na+)+c(H+)=c(OH-)+c(A-)
(2)②组情况表明,c>0.2mol•L-1(选填“>”、“<”或“=”).混合溶液中离子浓度c(A-)=c(Na+)(选填“>”、“<”或“=”)
(3)从③组实验结果分析,说明溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
12.下列做法不会对人体健康造成危害的是( )
| A. | 加三聚氰胺提高牛奶的含氮量 | |
| B. | 用苏丹红(色素)作食品着色剂 | |
| C. | 加小苏打(NaHCO3)作馒头的膨松剂 | |
| D. | 用含有甲醇(CH3OH)的工业酒精兑制饮用白酒 |
16.下列措施肯定使化学反应速率增大的是( )
| A. | 升高温度 | B. | 增加压强 | C. | 增大反应物的量 | D. | 使用催化剂 |
1.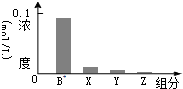 常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )
 常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )| A. | HA为强酸 | B. | 该混合溶液中:c(A-)+c(Y)=c(Na+) | ||
| C. | 图中X表示HA,Y表示H+,Z表示OH- | D. | 该混合液pH=7 |
8.从理论上讲,一切自发的氧化还原反应均可设计成原电池,下列不正确的是( )
| A. | 非自发的氧化还原反应不可以设计成原电池 | |
| B. | 将反应 3Cu+8HNO3═3Cu(NO3)2+2NO+4H2O 设计成原电池,其正极反应为:2NO3-+6e-+8H+═2NO+4H2O | |
| C. | 铅蓄电池工作时,正极、负极质量均增加 | |
| D. | 氢氧燃料电池耗H20.1mol时,电路中流经的电子数为0.1NA |
 2014年8月28日,第二届夏季青年奥林匹克运动会(以下简称“青奥会”)在南京奥体中心顺利闭幕.请完成下列与“青奥会”有关的填空.
2014年8月28日,第二届夏季青年奥林匹克运动会(以下简称“青奥会”)在南京奥体中心顺利闭幕.请完成下列与“青奥会”有关的填空.