题目内容
5.有100mL 0.2mol/L 的NaOH溶液,将此溶液稀释到200mL,则溶液中Na+的物质的量是0.02mol.分析 钠离子与氢氧化钠的浓度相等,根据稀释过程中溶质的物质的量不变进行计算稀释后溶液中Na+的物质的量.
解答 解:100mL 0.2mol/L 的NaOH溶液中含有氢氧化钠的物质的量为:0.2mol/L×0.1L=0.02mol,
稀释过程中钠离子的物质的量不变,则稀释后溶液中钠离子的物质的量仍然为0.02mol,
故答案为:0.02mol.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量与其它物理量之间的关系即可解答,注意稀释过程中钠离子的物质的量不变,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
13.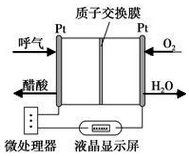 查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
 查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )| A. | 电流由呼气所在的铂电极流出 | |
| B. | O2所在的铂电极处发生还原反应 | |
| C. | 该电池工作一段时间后,正极区pH减小 | |
| D. | 该电池的负极反应式为:CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
10.已知酸性:H2SO3>H2S,下列实验操作后的反应液内肯定没有不溶物的是( )
| A. | 将SO2气体通入足量澄清石灰水 | |
| B. | 在Na2S溶液中通入SO2气体直至过过量 | |
| C. | 在Na2SO3溶液中通入H2S气体直至过量 | |
| D. | 将8.7克MnO2固体与含0.4mol溶质的浓盐酸加热并充分反应后 |
17.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | 熔点:CO2>KCl>SiO2 | B. | 水溶性:HCl>H2S>SO2 | ||
| C. | 沸点:NaH>H2O>H2S | D. | 硬度:SiC>石墨>CaCO3 |
14.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
| 选项 | 物质 | 试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| B | 苯(苯酚) | 饱和溴水 | 过滤 |
| C | 乙烷(乙烯) | 溴水 | 洗气 |
| D | 乙烯(二氧化硫) | 酸性高锰酸钾溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关物质应用的说法正确的是( )
| A. | 生石灰用作食品抗氧剂 | B. | 氢氧化铝用于制胃酸中和剂 | ||
| C. | 硫酸可作干燥剂 | D. | 氧化铁能用于制作吸铁石 |

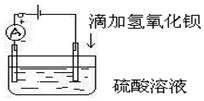 如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电性的关系.
如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电性的关系.