题目内容
①20g NaOH溶于水形成500mL溶液,所得溶液的物质的量浓度是 .
②标准状况下,44.8LNH3溶于水形成1L溶液,所得溶液的物质的量浓度是 .
③配制500mL 0.5mol?L-1的盐酸溶液,需要标准状况下的HCl气体 升.
②标准状况下,44.8LNH3溶于水形成1L溶液,所得溶液的物质的量浓度是
③配制500mL 0.5mol?L-1的盐酸溶液,需要标准状况下的HCl气体
考点:物质的量浓度的相关计算
专题:计算题
分析:①根据n=
计算20g NaOH的物质的量,再根据c=
计算所得溶液的物质的量浓度;
②根据n=
计算氨气的物质的量,再根据c=
计算所得溶液的物质的量浓度;
③根据n=cV计算HCl的物质的量,再根据V=nVm计算HCl的体积.
| m |
| M |
| n |
| V |
②根据n=
| V |
| Vm |
| n |
| V |
③根据n=cV计算HCl的物质的量,再根据V=nVm计算HCl的体积.
解答:
解:①20g NaOH的物质的量=
=0.5mol,溶于水形成500mL溶液,所得溶液的物质的量浓度=
=1mol/L,故答案为:1mol/L;
②标况下,44.8L氨气的物质的量=
=2mol,溶于水形成1L溶液,所得溶液的物质的量浓度=
=2mol/L,故答案为:2mol/L;
③HCl的物质的量=0.5L×0.5mol/L=0.25mol,标况下需要HCl的体积=0.25mol×22.4L/mol=5.6L,故答案为:5.6.
| 20g |
| 40g/mol |
| 0.5mol |
| 0.5L |
②标况下,44.8L氨气的物质的量=
| 44.8L |
| 22.4L/mol |
| 2mol |
| 1L |
③HCl的物质的量=0.5L×0.5mol/L=0.25mol,标况下需要HCl的体积=0.25mol×22.4L/mol=5.6L,故答案为:5.6.
点评:本题考查物质的量浓度有关计算,难度不大,注意对公式的理解与灵活应用.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
下列物质属于芳香烃的是( )
| A、乙醇 | B、乙酸 | C、乙苯 | D、硝基苯 |
 (1)如图所示装置,回答下列问题盐桥中阴离子移向
(1)如图所示装置,回答下列问题盐桥中阴离子移向 某化学兴趣小组的同学用以下装置研究电化学的问题.甲装置是由铜、锌和稀硫酸组成的原电池,其中正极材料是
某化学兴趣小组的同学用以下装置研究电化学的问题.甲装置是由铜、锌和稀硫酸组成的原电池,其中正极材料是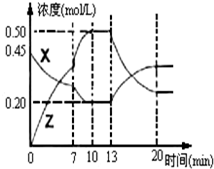 I.在1L容器中通入CO2、H2各2mol,在一定条件下发生反应:CO2+H2?CO+H2O,回答下列问题:
I.在1L容器中通入CO2、H2各2mol,在一定条件下发生反应:CO2+H2?CO+H2O,回答下列问题: ⑨CH≡CH.
⑨CH≡CH.