��Ŀ����
11�������й�˵����ȷ���ǣ�������| A�� | CaCO3��s���TCaO��s��+CO2��g�������²����Է����У�˵���÷�Ӧ�ġ�H��0 | |
| B�� | ȷ��ȡ24.00 mL��Һ���ѡ�õζ��ܡ���Ͳ��ζ��� | |
| C�� | N2��g��+3H2��g��?2NH3��g����H��0��������������ʱ�����¶ȣ���Ӧ����V��H2����������ƽ��ת���ʾ����� | |
| D�� | ��һ�ܱ������з���2SO2��g��+O2��g��?2SO3��g����Ӧ������ѹǿ��ƽ��������ƶ���$\frac{{c}^{2}��{SO}_{3}��}{{c}^{2}��{SO}_{2}��•c{��O}_{2}��}$ ��ֵ���� |
���� A����H-T��S��0�ķ�Ӧ�ܹ��Է����У�
B����Ͳ����С����Ϊ0.1mL��
C�������¶ȣ�ƽ�������ȷ����ƶ���
D������ѹǿƽ�������������С�ķ�����У�$\frac{{c}^{2}��S{O}_{3}��}{{c}^{2}��S{O}_{2}��c��{O}_{2}��}$�ǻ�ѧƽ�ⳣ���ļ������ʽ��ƽ�ⳣ�����¶ȱ仯��
��� �⣺A���÷�Ӧ�ġ�S��0�������²����Է����У�˵����H-T��S��0�����Ը÷�Ӧ�ġ�H��0����A��ȷ��
B����Ͳ����С����Ϊ0.1mL������������Ͳ��ȡ24.00mL����Һ������ʹ�õζ�����ȡ����B����
C��N2��g��+3H2��g��?2NH3��g����H��0����ӦΪ���ȷ�Ӧ�������¶�ƽ��Ӧ�����ȷ����ƶ������������ƶ���������ת���ʽ��ͣ���C����
D����һ�ܱ������з���2SO2��g��+O2��g��?2SO3��g����Ӧ������ѹǿ��ƽ��������ƶ���$\frac{{c}^{2}��S{O}_{3}��}{{c}^{2}��S{O}_{2}��c��{O}_{2}��}$�ǻ�ѧƽ�ⳣ���ļ������ʽ��ƽ�ⳣ�����¶ȱ仯������ѹǿ��ƽ�ⳣ�����䣬���ֵΪ���䣬��D����
��ѡA��
���� ���⿼���˷�Ӧ�Է����е����ݡ�������ȷ�ȡ���ѧƽ���ƽ�ⳣ�����㣬��Ҫ�ǻ�ѧƽ��ͷ�Ӧ����Ӱ�����أ���Ŀ�Ѷ��еȣ�

| A�� | ƽ�������ƶ��� | B�� | ����A��ת���ʼ�С�� | ||
| C�� | ����B���������������� | D�� | ��Ӧ����������v����v�� |
 ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����ش��������⣺
������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����ش��������⣺��1����֪C��s��+H2O��g��?CO��g��+H2��g������÷�Ӧ��ƽ�ⳣ������ʽΪ$\frac{c��CO��c��{H}_{2}��}{c��{H}_{2}O��}$��
��2����֪��һ���¶��£�
C��s��+CO2��g��?2CO��g����H1
CO��g��+H2O��g��?H2��g��+CO2��g����H2
C��s��+H2O��g��?CO��g��+H2��g����H3
���H1����H2����H3֮��Ĺ�ϵ�ǣ���H3=��H1+��H2���H1=��H3-��H2���H2=��H3-��H1��
��3��ͨ���о���ͬ�¶���ƽ�ⳣ�����Խ��ijЩʵ�����⣮��֪�������һ����̼��ˮ�������뷴Ӧʱ���ᷢ�����·�Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g�����÷�Ӧƽ�ⳣ�����¶ȵı仯�����ʾ��
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
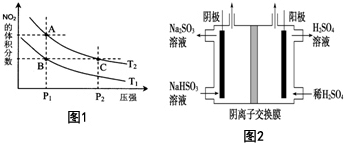
��4���Ӱ����������������ᣬ�˹������漰���������NO��NO2��N2O4�ȣ��Է�ӦN2O4��g��?2NO2��g����H��0���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ1��ʾ������˵����ȷ����E��
A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬A��״̬B�������ü��ȵķ���
E��A��C����Ļ�ѧƽ�ⳣ����A=C
��5����ҵ����Na2SO3����β���е�SO2������ͼ2װ�õ�⣨���Ե缫��NaHSO3��ȡH2SO4�������ӽ���Ĥֻ����������ͨ�����������缫��ӦʽΪ��HSO3-+H2O-2e-=SO42-+3H+���������ݳ�����ijɷ�ΪO2��SO2���ѧʽ����
| A�� | Cl2��FeBr2��Һ��Ӧ����n��Cl2����n��FeBr2��=1��1ʱ��2Fe2++4Br-+3Cl2�T2Fe2++2Br2+6Cl- | |
| B�� | NaOH��Һ��SO2��Ӧ����n��NaOH����n��SO2��=4��3ʱ��4OH-+3SO2�TSO32-+2HSO3-+H2O | |
| C�� | ��̪����̼������Һ�У���Һ��죺CO32-+H2O�THCO3-+OH- | |
| D�� | ������Ͷ��NaOH��Һ�У�Al+OH-+H2O�TAlO2-+H2�� |
 bB��g��+cC��g�������¶Ȳ���������£��ٳ���һ������A�����´ﵽƽ��ʱ�������ж�����ȷ���ǣ� ��
bB��g��+cC��g�������¶Ȳ���������£��ٳ���һ������A�����´ﵽƽ��ʱ�������ж�����ȷ���ǣ� ��