题目内容
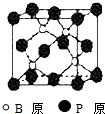 磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.
磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.回答下列问题:
(1)上述反应物中含有一种元素,其基态原子具有八种不同能量电子,写出其基态原子的价电子轨道表示式
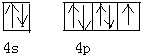 .
.(2)BP中每个B或P原子均形成4个共价键,其中有一个配位键,提供空轨道是
(3)磷化硼的晶体类型是
(4)已知BBr3+PBr3+3H2=BP+6HBr反应中,P元素被还原,判断电负性:P
(5)BBr3分子中,B原子采取
(6)氮化硼晶体的熔点要比磷化硼晶体高,其原因是
考点:晶胞的计算,原子核外电子排布,晶体的类型与物质熔点、硬度、导电性等的关系,原子轨道杂化方式及杂化类型判断
专题:原子组成与结构专题,化学键与晶体结构
分析:(1)其基态原子具有八种不同能量电子,该原子的能级有1S、2S、2P、3S、3P、3d、4S、4P,据此确定该元素;
(2)没有孤电子对的原子提供空轨道;
(3)根据其空间结构确定晶体类型,根据每个B原子含有的价层电子对个数确定杂化方式,根据每个B原子含有的B-P键个数计算;
(4)得电子能力越强的元素其电负性越强;
(5)根据电子对互斥理论确定其空间构型,根据空间构型确定键角;
(6)原子晶体中,物质熔点与原子半径、键长成反比.
(2)没有孤电子对的原子提供空轨道;
(3)根据其空间结构确定晶体类型,根据每个B原子含有的价层电子对个数确定杂化方式,根据每个B原子含有的B-P键个数计算;
(4)得电子能力越强的元素其电负性越强;
(5)根据电子对互斥理论确定其空间构型,根据空间构型确定键角;
(6)原子晶体中,物质熔点与原子半径、键长成反比.
解答:
解:(1)其基态原子具有八种不同能量电子,该原子的能级有1S、2S、2P、3S、3P、3d、4S、4P,所以该元素是第四周期的P区元素,为Br元素,其基态原子的价电子轨道表示式 ,故答案为:
,故答案为: ;
;
(2)没有孤电子对的原子提供空轨道,B原子没有孤电子对,所以提供空轨道,P原子提供孤电子对,故答案为:B;
(3)根据其根据结构知,该物质为空间网状结构,所以是原子晶体,每个B原子含有4个σ键不含孤电子对,所以采取sp3杂化,每个B原子含有4个B-P键,所以每生成1molBP,共形成4molB-P键,故答案为:原子晶体,sp3;4;
(4)BBr3+PBr3+3H2=BP+6HBr反应中,P元素被还原,则P元素得电子能力比B元素强,得电子能力越强的元素其电负性越强,所以电负性P>B,故答案为:>;
(5)BBr3分子中,B原子含有3个σ键不含孤电子对,所以采取sp2杂化,为平面三角形结构,键角是120℃,故答案为:sp2;120°;
(6)原子晶体中,物质熔点与原子半径、键长成反比,磷原子的半径比氮原子大,N-B共价键键长比B-P小,键能大,所以氮化硼晶体的熔点要比磷化硼晶体高,
故答案为:磷原子的半径比氮原子大,N-B共价键键长比B-P小,键能大.
 ,故答案为:
,故答案为: ;
;(2)没有孤电子对的原子提供空轨道,B原子没有孤电子对,所以提供空轨道,P原子提供孤电子对,故答案为:B;
(3)根据其根据结构知,该物质为空间网状结构,所以是原子晶体,每个B原子含有4个σ键不含孤电子对,所以采取sp3杂化,每个B原子含有4个B-P键,所以每生成1molBP,共形成4molB-P键,故答案为:原子晶体,sp3;4;
(4)BBr3+PBr3+3H2=BP+6HBr反应中,P元素被还原,则P元素得电子能力比B元素强,得电子能力越强的元素其电负性越强,所以电负性P>B,故答案为:>;
(5)BBr3分子中,B原子含有3个σ键不含孤电子对,所以采取sp2杂化,为平面三角形结构,键角是120℃,故答案为:sp2;120°;
(6)原子晶体中,物质熔点与原子半径、键长成反比,磷原子的半径比氮原子大,N-B共价键键长比B-P小,键能大,所以氮化硼晶体的熔点要比磷化硼晶体高,
故答案为:磷原子的半径比氮原子大,N-B共价键键长比B-P小,键能大.
点评:本题考查了物质结构的综合性知识,原子的杂化方式、分子的空间构型、键角等知识点是高考的热点,应重点掌握.

练习册系列答案
相关题目
相同状况下,下列气体所占体积最大的是( )
| A、80g SO3 |
| B、3g H2 |
| C、16g O2 |
| D、34g H2S |
以下四种物质,其中A、B各代表一种离子晶体的晶胞,C代表一种合金的晶胞,D则代表一个由A、B原子组成的团簇分子,其中化学式错误的是( )
A、 AB |
B、 XY3Z |
C、 EF |
D、 AB |
下列离子方程式不正确的是( )
| A、碳酸钡与盐酸反应:BaCO3+2H+═Ba2++CO2↑+H2O |
| B、金属铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| D、NaHCO3溶液与NaOH溶液混合:HCO3-+OH-═CO32-+H2O |
能除去空气中氧气,且不生成其他气体的是( )
| A、木炭 | B、红磷 | C、硫 | D、铁丝 |
只用胶头滴管和试管,不用其他试剂就可以区别的下列溶液(浓度均为0.1mol/L)是( )
| A、CaCl2和Na2CO3 |
| B、稀H2SO4和NaHCO3 |
| C、Ba(OH)2和NaHCO3 |
| D、NaAlO2和盐酸 |
 如图所示中各物质均为中学化学中常见的物质,它们之间有如图转化关系.其中A、C均为金属单质;D的焰色反应呈黄色;C与水反应除了生成D,还能生成自然界最轻的气体;E是一种氢氧化物,它既能跟NaOH反应又能跟盐酸反应.(反应过程中生成的水及其他产物已略去)
如图所示中各物质均为中学化学中常见的物质,它们之间有如图转化关系.其中A、C均为金属单质;D的焰色反应呈黄色;C与水反应除了生成D,还能生成自然界最轻的气体;E是一种氢氧化物,它既能跟NaOH反应又能跟盐酸反应.(反应过程中生成的水及其他产物已略去)