题目内容
在一个温度恒定的密闭容器中发生反应2SO2+O2?2SO3,请按要求回答下列问题.
[恒定压强条件下]
(1)若开始时放入1mol SO2和0.5mol O2,达平衡后,生成0.9mol SO3,这时SO2的转化率为 .
(2)若开始时放入4mol SO2和2mol O2,达平衡后,生成SO3的物质的量为 .
[恒定容积条件下]
(3)若开始时放入1mol SO2和0.5mol O2,达平衡后,生成a mol SO3,则a 0.9(填“>”、“<”或“=”).
[恒定压强条件下]
(1)若开始时放入1mol SO2和0.5mol O2,达平衡后,生成0.9mol SO3,这时SO2的转化率为
(2)若开始时放入4mol SO2和2mol O2,达平衡后,生成SO3的物质的量为
[恒定容积条件下]
(3)若开始时放入1mol SO2和0.5mol O2,达平衡后,生成a mol SO3,则a
考点:化学平衡的计算
专题:化学平衡专题
分析:恒定压强条件下:1molSO2和0.5molO2与4molSO2和2molO2的比值相等,应为等效平衡状态,两种平衡状态下各物质的含量相等,可利用三段式法解答;
恒定容积条件下:随着反应的进行,容器内压强逐渐减小,与恒定压强条件下相比,SO2的转化率小于(1)中SO2的转化率.
恒定容积条件下:随着反应的进行,容器内压强逐渐减小,与恒定压强条件下相比,SO2的转化率小于(1)中SO2的转化率.
解答:
解:(1)SO2+O2 ?2SO3
起始(mol) 1 0.5 0
转化(mo1)x 0.5x x
平衡(mol) 1-x 0.5-0.5x 0.9
由题意知:x=0.9
则SO2的转化率=
×l00%=90%,
故答案为:90%;
(2)在恒压条件下,此平衡与(1)中的平衡为等效平衡,各物质的含量相等,转化率相等,则有达平衡后,生成SO3的物质的量为4mol×90%=3.6mol,故答案为:3.6mol;
(3)由于正反应为气体体积变小的反应,则在恒容条件下,随反应的进行,容器内压强逐渐变小,故此条件下,SO2的转化率小于(1)中SO2的转化率(90%),推导出SO3小于0.9mol,
故答案为:<.
起始(mol) 1 0.5 0
转化(mo1)x 0.5x x
平衡(mol) 1-x 0.5-0.5x 0.9
由题意知:x=0.9
则SO2的转化率=
| 0.9mol |
| 1mol |
故答案为:90%;
(2)在恒压条件下,此平衡与(1)中的平衡为等效平衡,各物质的含量相等,转化率相等,则有达平衡后,生成SO3的物质的量为4mol×90%=3.6mol,故答案为:3.6mol;
(3)由于正反应为气体体积变小的反应,则在恒容条件下,随反应的进行,容器内压强逐渐变小,故此条件下,SO2的转化率小于(1)中SO2的转化率(90%),推导出SO3小于0.9mol,
故答案为:<.
点评:题考查化学平衡的计算,题目难度不大,注意根据三段式法计算较为直观,本题要特别注意(1)与(2)在等压下为等效平衡状态,为解答该题的关键,也是易错点.

练习册系列答案
相关题目
下列说法正确的是( )
| A、将浓度为0.1mol?L-1 HF溶液加水不断稀释过程中,c( H+) 和c ( OH-)都会减小 |
| B、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的PH.若PH>7,则H2A是弱酸;若PH<7,则H2A是强酸 |
| C、将SO2通入一定量KOH溶液,所得溶液呈中性,该溶液中一定含KHSO3 |
| D、用0.200mol?L-1 NaOH标准溶液滴定浓度均为0.1mol?L-1 的HCl与CH3COOH的混合液,至中性时,溶液中的酸恰好被完全中和 |
在无土栽培中,需配制一定量含50mol NH4Cl、6mol KCl和24mol K2SO4的营养液.若用KCl、NH4Cl、(NH4)2SO4为原料来配制此营养液,三者的物质的量依次是( )mol.
| A、2、54、24 |
| B、54、2、24 |
| C、32、50、12 |
| D、16、50、24 |
不属于氧化还原反应的是( )
A、8Al+3Fe3O4
| ||||
B、2Mg+CO2
| ||||
C、N2+3H2
| ||||
D、SiO2+CaO
|
 雪花,被人们称为“冬之精灵”,科学研究发现,世界上没有两片雪花的形状完全相同的.下列有关说法正确的是( )
雪花,被人们称为“冬之精灵”,科学研究发现,世界上没有两片雪花的形状完全相同的.下列有关说法正确的是( )| A、在雪花的形成过程中,水分子由运动变为静止 |
| B、雪花融化时,水分子之间的间隔没有发生变化 |
| C、不同雪花中,水分子化学性质不相同 |
| D、不同雪花中,水分子数目都是巨大的 |


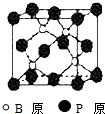 磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.
磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.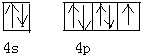 .
.