题目内容
以下四种物质,其中A、B各代表一种离子晶体的晶胞,C代表一种合金的晶胞,D则代表一个由A、B原子组成的团簇分子,其中化学式错误的是( )
A、 AB |
B、 XY3Z |
C、 EF |
D、 AB |
考点:晶胞的计算
专题:化学键与晶体结构
分析:离子晶体和金属晶体中利用均摊法计算晶胞中含有的离子或原子个数确定其化学式,团簇分子中含有的原子个数即是该分子独有的,注意不能用均摊法计算.
解答:
解:A.该晶胞中含有的A离子个数为1,B离子个数=
×8=1,A、B离子个数之比是1:1,所以其化学式为AB,故A正确;
B.该晶胞中含有X离子个数为1,Y离子个数=
×6=3,Z离子个数=
×8=1,所以其化学式为XY3Z,故B正确;
C.该晶胞中E原子个数=
×4=
,F原子个数═
×4=
,E、F原子之比为1:1,所以其化学式为EF,故C正确;
D.该团簇分子中所有的原子被其独自占有,所以A原子个数=14,B原子个数=12,所以其化学式为A14B12,故D错误;
故选D.
| 1 |
| 8 |
B.该晶胞中含有X离子个数为1,Y离子个数=
| 1 |
| 2 |
| 1 |
| 8 |
C.该晶胞中E原子个数=
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
D.该团簇分子中所有的原子被其独自占有,所以A原子个数=14,B原子个数=12,所以其化学式为A14B12,故D错误;
故选D.
点评:本题考查了晶胞的计算,对于离子晶体采用均摊法计算确定化学式,注意团簇分子中所有的原子被该分子独自占有,不能用均摊法计算,为易错点.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列物质都能导电,其中属于电解质的是( )
| A、稀盐酸 | B、熔融的NaCl |
| C、铜丝 | D、NaOH溶液 |
在无土栽培中,需配制一定量含50mol NH4Cl、6mol KCl和24mol K2SO4的营养液.若用KCl、NH4Cl、(NH4)2SO4为原料来配制此营养液,三者的物质的量依次是( )mol.
| A、2、54、24 |
| B、54、2、24 |
| C、32、50、12 |
| D、16、50、24 |
不属于氧化还原反应的是( )
A、8Al+3Fe3O4
| ||||
B、2Mg+CO2
| ||||
C、N2+3H2
| ||||
D、SiO2+CaO
|
用NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A、常温常压下,22.4L氢气中含有的氢分子数为NA |
| B、24gMg变为Mg2+时失去的电子数为2 NA |
| C、32g臭氧分子中含有的氧原子数为2 NA |
| D、1L1mol/LCaCl2溶液中含有氯离子数为2 NA |
 图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料.根据图示回答问题:
图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料.根据图示回答问题: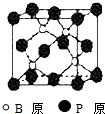 磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.
磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr. .
. 如图,做铁丝在氧气里燃烧的实验时,集气瓶里放入少量水的作用是
如图,做铁丝在氧气里燃烧的实验时,集气瓶里放入少量水的作用是