题目内容
无土栽培技术研究配制一种营养液,此1L营养液中含0.5molNH4Cl、0.16molKCl、0.24molK2SO4.若用KCl、NH4Cl和(NH4)2SO4三种固体来配制,则每升溶液中需三种固体的物质的量依次为( )
| A、0.32mol、0.5mol、0.12mol |
| B、0.02mol、0.64mol、0.24mol |
| C、0.64mol、0.02mol、0.24mol |
| D、0.16mol、0.5mol、0.24mol |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:根据n=cV计算各物质的物质的量,进而计算混合液中各离子的物质的量,再根据离子守恒可知,n[(NH4)2SO4]=n(SO42-),n( KCl)=n( K+ ),n(NH4Cl)+n(KCl)=n( Cl- ),据此计算解答.
解答:
解:0.5mol NH4Cl、0.16mol KCl、0.24mol K2SO4中 n(NH4+)=n(NH4Cl)=0.5mol;
n( Cl- )=n(NH4Cl)+n( KCl)=0.5mol+0.16mol=0.66mol;
n( K+ )=n( KCl)+2n( K2SO4)=0.16mol+2×0.24mol=0.64mol;
n(SO42-)=n( K2SO4)=0.24mol;
用KCl、NH4Cl、(NH4)2SO4配制,
n((NH4)2SO4)=n(SO42-)=0.24mol;
n( KCl)=n( K+ )=0.64mol;
n(NH4Cl)=n( Cl- )-n( KCl)=0.66mol-0.64mol=0.02mol;
三种固体的物质的量为:0.64mol、0.02mol、0.24mol,
故选C.
n( Cl- )=n(NH4Cl)+n( KCl)=0.5mol+0.16mol=0.66mol;
n( K+ )=n( KCl)+2n( K2SO4)=0.16mol+2×0.24mol=0.64mol;
n(SO42-)=n( K2SO4)=0.24mol;
用KCl、NH4Cl、(NH4)2SO4配制,
n((NH4)2SO4)=n(SO42-)=0.24mol;
n( KCl)=n( K+ )=0.64mol;
n(NH4Cl)=n( Cl- )-n( KCl)=0.66mol-0.64mol=0.02mol;
三种固体的物质的量为:0.64mol、0.02mol、0.24mol,
故选C.
点评:本题考查溶液配制的基本原则,题目难度不大,原溶液中离子物质的量和配制溶液中的离子物质的量相同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法错误的是( )
| A、所有金属元素都可以用焰色反应来确定其存在 |
| B、三位美国科学家因给复杂化学体系设计多尺度模型面共享了2013年诺贝尔化学奖 |
| C、已知PM2.5是指大气中直径≤2.5微米的颗粒物,对人体健康危害很大 |
| D、借助仪器来分析化学物质的组成是常用的手段,原子吸收光谱常用来确定物质中含有哪些金属元素 |
关于如图所示装置的下列叙述,正确的是( )
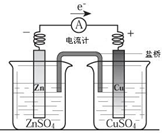

| A、电流方向是从锌片经导线流向铜片 |
| B、锌是阳极,锌片上有大量气泡产生 |
| C、铜离子在铜片表面被氧化,质量逐渐增大 |
| D、盐桥作用主要是离子通道和保持溶液电中性 |
NaHCO3溶液中所含有的分子和离子有( )
①NaHCO3 ②H2O ③H2CO3 ④HCO3- ⑤H+ ⑥OH-⑦CO32-.
①NaHCO3 ②H2O ③H2CO3 ④HCO3- ⑤H+ ⑥OH-⑦CO32-.
| A、①②③ |
| B、②④⑤⑥ |
| C、②③④⑤⑥⑦ |
| D、①②③④⑤⑥⑦ |
下列有关说法正确的是( )
| A、C.用0.2000 mol/L NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1 mol/L),至中性时,溶液中的酸未被完全中和 |
| B、常温下,反应2A (s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0 |
| C、N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大 |
| D、水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
反应2NO+2CO
N2+2CO2可应用于汽车尾气的净化.下列判断正确的是( )
| ||
| A、该反应是置换反应 |
| B、该反应是复分解反应 |
| C、CO是氧化剂 |
| D、NO发生还原反应 |