题目内容
使H2SO4与过量Zn反应速率下降但不影响H2 的量,应加入( )
| A、Na2CO3 (s) |
| B、(NH4)2SO4 (s) |
| C、K2SO4 (aq) |
| D、H2O (l) |
| E、CH3COONa(s) |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:反应的实质为Zn+2H+═Zn2++H2↑,为了减缓反应速率,但又不影响生成氢气的总量,则减小氢离子的浓度但不能改变氢离子的物质的量即可,以此来解答.
解答:
解:A.碳酸钠消耗硫酸,生成氢气的量减少,故A错误;
B.硫酸铵溶液水解呈酸性,生成氢气的量增多,故B错误;
C.加入K2SO4 溶液,与锌不反应,溶液体积增大,氢离子浓度减小,反应速率减小,故C正确;
D.加水体积增大,氢离子浓度减小,反应速率减小,生成氢气的总量不变,故D正确;
E.加入醋酸钠,生成弱酸,氢离子浓度降低,反应速率减小,氢气的总量不变,故E正确.
故选CDE.
B.硫酸铵溶液水解呈酸性,生成氢气的量增多,故B错误;
C.加入K2SO4 溶液,与锌不反应,溶液体积增大,氢离子浓度减小,反应速率减小,故C正确;
D.加水体积增大,氢离子浓度减小,反应速率减小,生成氢气的总量不变,故D正确;
E.加入醋酸钠,生成弱酸,氢离子浓度降低,反应速率减小,氢气的总量不变,故E正确.
故选CDE.
点评:本题考查化学反应速率的影响因素,侧重于基础知识的考查,注意把握影响化学反应速率的因素,把握题目要求,为解答该题的关键,难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
已知某氧化剂XO3-中+5价的X能被Na2SO3还原成0价,则还原含有2.4×10-3molXO3-的溶液,需0.2mol?L-1的Na2SO3溶液的体积为( )
| A、40mL | B、30mL |
| C、20mL | D、10mL |
体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01mol,下列叙述正确的是( )
| A、醋酸溶液的pH大于盐酸 |
| B、醋酸溶液的pH小于盐酸 |
| C、与NaOH完全中和时,醋酸消耗的NaOH多于盐酸 |
| D、分别用水稀释相同倍数后,所得溶液中:n (Cl-)=n (CH3COO-) |
下列各组物质的分类正确的是( )
| 选项 | 电解质 | 纯净物 | 碱性氧化物 | 酸性氧化物 |
| A | 酒精溶液 | 冰水混合物 | CaO | SO2 |
| B | BaSO4 | 液氯 | Fe2O3 | CO2 |
| C | Fe(OH)3 | CuSO4?5H2O | Al2O3 | SO2 |
| D | NH3 | 水银 | CuO | NO2 |
| A、A | B、B | C、C | D、D |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、1 mol Cl2与足量的铁反应转移的电子数是2 NA |
| B、常温常压下22.4 L HCl气体含有的分子数是NA |
| C、0.1 mol/L CuCl2溶液中Cl-数目是0.2 NA |
| D、32 g O2中含有的原子数是 NA |
下列对Na2CO3与NaHCO3的描述正确的是( )
| A、Na2CO3比NaHCO3的溶度大 |
| B、受热时NaHCO3比Na2CO3稳定 |
| C、澄清的石灰水能与Na2CO3反应而不与NaHCO3反应 |
| D、向相同浓度的NaHCO3与Na2CO3溶液中分别滴入2滴酚酞溶液,前者红色更深 |
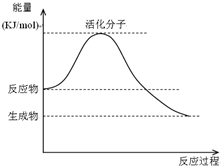 (1)如图是某化学反应中的能量变化图.
(1)如图是某化学反应中的能量变化图.