题目内容
2.请填写相应物质的编号:①Fe2O3 ②Fe3O4 ③KAl(SO4)2•12H2O ④Si ⑤SiO2水晶、玛瑙的主要成份是⑤;常用作红色油漆和涂料的物质是①;易与水生成胶体,常用作净水剂的是③.
分析 玛瑙、水晶、石英钟表的主要成份都是二氧化硅;氧化铁俗称铁红,常用作红色油漆和涂料;明矾是常用的净水剂,是利用了明矾溶于水后生成的胶状物对杂质的吸附,使悬浮于水中的杂质沉降.
解答 解:玛瑙、水晶的主要成份都是二氧化硅;常用作红色油漆和涂料的物质是氧化铁;易与水生成胶体,常用作净水剂的是明矾;故答案为:⑤;①;③.
点评 本题难度不大,考查水的净化、水晶、玛瑙的成份,掌握水的净化的原理、氧化铁红色染料是正确解答本题的关键.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
13.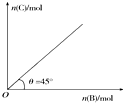 盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )
盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )
 盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )
盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )| A. | 降低温度,则图中θ>45° | |
| B. | 平衡后再加入B,正反应速率增大,逆反应速率减小 | |
| C. | 平衡时B的转化率为50% | |
| D. | 平衡后再加入A,体系内气体密度不变 |
10.氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:a HClO3→b O2↑+c Cl2↑+d HClO4+e H2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色.下列说法错误的是( )
| A. | 由反应可确定:氧化性HClO3>HClO4 | |
| B. | 变蓝的淀粉碘化钾试纸褪色是因为可能发生了:4C12+I2+6H2O→12H++8Cl-+2IO3- | |
| C. | 若氯酸分解所得的混合气体的平均摩尔质量为47.6g/mol,则反应方程式可表示为:26HClO3→15O2↑+8C12↑+10HClO4+8H2O | |
| D. | 若化学计量数a=8,b=3,则该反应转移电子数为20e |
17.将分别通入下列种溶液中,有关说法正确的是( )
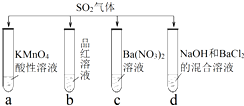

| A. | 试管a中实验可以证明具有漂白性 | |
| B. | 试管b中溶液褪色,说明具有强氧化性 | |
| C. | 试管c中能产生白色沉淀,说明具有还原性 | |
| D. | 试管d中能产生白色沉淀,该沉淀完全溶于 稀硝酸 |
7.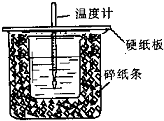 已知中和热的定义为:稀溶液中酸和碱发生中和反应生成1mol水的反应热,某化学兴趣小组要完成中和热的测定实验,装置如右图,回答下列问题:
已知中和热的定义为:稀溶液中酸和碱发生中和反应生成1mol水的反应热,某化学兴趣小组要完成中和热的测定实验,装置如右图,回答下列问题:
(1)从如图实验装置看,其中尚缺少的一种玻璃仪器的名称是
环形玻璃搅拌棒,碎纸条的作用是减少实验过程中的热量损失,如果大烧杯上不盖硬纸板,实验所测得的中和热会偏大(填“偏大”、“偏小”或“无影响”).
(2)实验数据记录如下表(t1为混合前两溶液平均温度,t2为混合充分反应后读取的温度):
①已知反应后溶液的比热容为4.18J•℃-1•g-1,各溶液密度均近似为1g•cm-3,计算完成上表(保留一位小数,将结果填写在表格中横线上)
②强酸与强碱反应的中和热理论值为-57.3kJ•mol-1,下面列举的情况中可能造成上述实验结果与理论值的差距的是ABC(填字母序号)
A.倒入反应溶液时有少许溅出
B.倒入NaOH溶液时速度缓慢
C.未在温度达到最高点时读数
③现用一定量的稀氢氧化钾溶液、澄清石灰水代替氢氧化钠溶液,分别与上述实验的盐酸恰好完全反应时的反应热分别为△H1、△H2,则理论上两者的大小关系为:△H1=△H2(填“<”“>”或“=”)
 已知中和热的定义为:稀溶液中酸和碱发生中和反应生成1mol水的反应热,某化学兴趣小组要完成中和热的测定实验,装置如右图,回答下列问题:
已知中和热的定义为:稀溶液中酸和碱发生中和反应生成1mol水的反应热,某化学兴趣小组要完成中和热的测定实验,装置如右图,回答下列问题:(1)从如图实验装置看,其中尚缺少的一种玻璃仪器的名称是
环形玻璃搅拌棒,碎纸条的作用是减少实验过程中的热量损失,如果大烧杯上不盖硬纸板,实验所测得的中和热会偏大(填“偏大”、“偏小”或“无影响”).
(2)实验数据记录如下表(t1为混合前两溶液平均温度,t2为混合充分反应后读取的温度):
| 实 验 用 品 | 溶液温度(℃) | 中和热△H(kJ•mol-1) | |||
| t1 | t2 | ||||
| ① | 50 mL 0.50 mol•L-1NaOH | 50 mL 0.50 mol•L-1HCl | 20 | 23.3 | -56.8 |
| ② | 50 mL 0.50 mol•L-1NaOH | 50 mL 0.50 mol•L-1HCl | 20 | 23.5 | |
②强酸与强碱反应的中和热理论值为-57.3kJ•mol-1,下面列举的情况中可能造成上述实验结果与理论值的差距的是ABC(填字母序号)
A.倒入反应溶液时有少许溅出
B.倒入NaOH溶液时速度缓慢
C.未在温度达到最高点时读数
③现用一定量的稀氢氧化钾溶液、澄清石灰水代替氢氧化钠溶液,分别与上述实验的盐酸恰好完全反应时的反应热分别为△H1、△H2,则理论上两者的大小关系为:△H1=△H2(填“<”“>”或“=”)
11.下列离子方程式正确的是( )
| A. | 用Al作电极电解NaHCO3溶液:2Al+6H2O═2Al(OH)3↓+3H2↑ | |
| B. | 向明矾溶液中加入氢氧化钡溶液至沉淀质量最大时:2Al3++2SO42-+2Ba2++6OH-═2BaSO4↓+2Al(OH)3↓ | |
| C. | 碳酸钠的水解反应:CO32-+H3O+═HCO3-+H2O | |
| D. | 酸性高锰酸钾溶液与双氧水反应:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
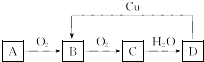
 ;反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O;已知反应II的产物X的溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为2S2-+5H2O=S2O32-+4H2↑+2OH-.
;反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O;已知反应II的产物X的溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为2S2-+5H2O=S2O32-+4H2↑+2OH-.
 密闭容器中,能说明反应:2N02(g)
密闭容器中,能说明反应:2N02(g) 2NO(g)+02(g)达到平衡
2NO(g)+02(g)达到平衡 状态的是 ( )
状态的是 ( )