题目内容
13.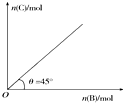 盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )
盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )| A. | 降低温度,则图中θ>45° | |
| B. | 平衡后再加入B,正反应速率增大,逆反应速率减小 | |
| C. | 平衡时B的转化率为50% | |
| D. | 平衡后再加入A,体系内气体密度不变 |
分析 根据在一定温度、压强下达到平衡,平衡时C的物质的量与加入B的物质的量的变化关系图可知,平衡时再加入B,因体积可变,则B的浓度不变,则平衡后B的加入平衡不移动;该反应是放热反应,当降低温度时,平衡向放热方向移动,平衡正向移动,则C的物质的量增加;再由图可知,达平衡时B、C的物质的量相等来计算B的转化率.
解答 解:A、压强一定,当降低温度时,平衡向放热方向移动,平衡正向移动,则C的物质的量增加,由图可以看出,图中α将变大,图中θ>45°,故A正确;
B、因体积不变,平衡后再加入B,正反应速率增大,逆反应速率增大,故B错误;
C、根据图象结合方程式知,加入的B物质的物质的量与生成C物质的物质的量相等,所以该反应中有一半的B物质反应,所以其转化率为50%,故C正确;
D、因体积不变,平衡后再加入A,平衡不移动,气体的质量不变,体系内气体密度不变,故D正确;
故选B.
点评 本题考查化学平衡的图象分析,明确图象中的纵横坐标含有及隐含平衡时的信息是解答的关键,并利用影响化学反应速率及化学平衡的影响因素来解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)═4NO2(g)+O2(g)△H>0.一定温度时,向密闭容器中通入N2O5,部分实验数据见表:下列说法中错误的是( )
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
| A. | 500s时O2的浓度为0.075mol/L | |
| B. | 平衡后,升高温度,正反应速率先增大后减小 | |
| C. | 平衡后,要使平衡常数增大,改变的条件是升高温度 | |
| D. | 1000s时将容器的体积缩小一半,重新达到平衡时0.25mol/L<c(N2O5)<0.50mol/L |
1.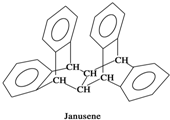 如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,下列说法正确的是( )
如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,下列说法正确的是( )
 如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,下列说法正确的是( )
如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,下列说法正确的是( )| A. | Janusene的分子式为C30H20 | |
| B. | Janusene属于苯的同系物 | |
| C. | Janusene苯环上的一氯代物有8种 | |
| D. | Janusene既可发生氧化反应,又可发生还原反应 |
8.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 22.4LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 标准状况下,22.4L氩气含有原子数为2Na | |
| C. | 常温常压下,32g O2和O3混合气所含氧原子数是2NA | |
| D. | 物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数为1NA |
18.某NaHCO3和Na2CO3•xH2O的混合物40g,在200℃下,对其加热不再产生气体为止,得到固体21.2g.再把加热过程中产生的气体全部通入含有0.05mol Ca(OH)2的溶液中,恰好使生成的沉淀完全消失,则x为( )
| A. | 6 | B. | 7 | C. | 9 | D. | 10 |
5.能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应原理为:CO(g)+2H2(g)═CH3OH(g)△H,如表所列数据是该反应在不同温度下的化学平衡常数(K).
(1)根据表中数据可判断△H<0 (填“>”、“=”或“<”).
(2)在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断.
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(2)在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断.
2.请填写相应物质的编号:①Fe2O3 ②Fe3O4 ③KAl(SO4)2•12H2O ④Si ⑤SiO2
水晶、玛瑙的主要成份是⑤;常用作红色油漆和涂料的物质是①;易与水生成胶体,常用作净水剂的是③.
水晶、玛瑙的主要成份是⑤;常用作红色油漆和涂料的物质是①;易与水生成胶体,常用作净水剂的是③.
3.根据反应:2KClO3+I2═2KIO3+Cl2↑判断,下列结论不正确的是( )
| A. | 该反应属于置换反应 | B. | I2具有还原性 | ||
| C. | 当生成1mol Cl2时转移2mol电子 | D. | 氧化剂是KClO3 |

 .
. .
. )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下:
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下: .
.