题目内容
19.下列说法正确的是( )| A. | SO2通入BaCl2溶液中无现象,加入氨水后得到BaSO4沉淀 | |
| B. | SO2通入酸性KMnO4溶液中,溶液褪色,体现SO2的漂白性 | |
| C. | SO2通入紫色石蕊试液中,溶液变红色 | |
| D. | 等物质的量的SO2和Cl2通入水中,溶液的漂白性增强 |
分析 A、盐酸酸性强亚硫酸,所以SO2通入BaCl2溶液不反应,加入氨水生成亚硫酸钡;
B、向酸性KMnO4溶液中通入SO2,发生氧化还原反应生成硫酸根离子;
C、二氧化硫为酸性氧化性,生成亚硫酸;
D、二氧化硫与氯气等物质的量通入水中发生化学反应:SO2 +Cl2 +2H2O=H2SO4+2HCl,依据生成物的性质解答.
解答 解:A、盐酸酸性强亚硫酸,所以SO2通入BaCl2溶液不反应,加入氨水生成亚硫酸钡,而不是硫酸钡,故A错误;
B、向酸性KMnO4溶液中通入SO2,发生氧化还原反应生成硫酸根离子,S元素的化合价升高,是SO2的还原性,而不是SO2的漂白性,故B错误;
C、二氧化硫为酸性氧化性,生成亚硫酸,所以SO2通入紫色石蕊试液中,溶液变红色,故C正确;
D、将等物质的量的SO2、CI2通入水中发生化学反应:SO2 +Cl2+2H2O=H2SO4+2HCl,生成物硫酸、氯化氢电离产生氢离子,溶液显酸性,不具有漂白性,故D错误;
故选C.
点评 本题考查了物质的性质,明确二氧化硫、氯气发生的化学反应是解题关键,题目难度不大.

练习册系列答案
相关题目
18.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 9 g超重水(3H216O)含中子数为6NA | |
| B. | 标准状况下,22.4 L CCl4含有的分子数目为NA | |
| C. | 常温常压下,16g甲烷中共价键数目为4NA | |
| D. | 1 L 0.1 mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA |
19.化学知识在生产和生活中有重要的应用,下列说法中不正确的是( )
| A. | 发酵粉中含有NaHCO3,能使焙制出的糕点疏松多孔 | |
| B. | 利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程 | |
| C. | 鼓励利用太阳能,风能等清洁能源,可以减少PM2.5的污染 | |
| D. | 金属钠、金属镁等活泼金属着火时,可以使用泡沫灭火器来灭火 |
7.下列离子方程式中不正确的是( )
| A. | 氢氧化钡溶液和硫酸钠溶液混合:Ba2++SO42-=BaSO4↓ | |
| B. | 将亚硫酸氢钠加入盐酸溶液中:HSO3-+H+=SO2↑+H2O | |
| C. | 氢硫酸与亚硫酸混合:H2SO3+2H2S=3S↓+3H2O | |
| D. | H2S气体通入CuSO4溶液中:Cu2++S2-=CuS↓ |
14.检验制得的HCl气体中混有少量Cl2的方法是( )
| A. | 观察气体的颜色 | B. | 用干燥的蓝色石蕊试纸 | ||
| C. | 用硝酸银溶液 | D. | 用湿润的淀粉碘化钾试纸 |
4.下列物质均有漂白作用,但其中一种的漂白原理与其它三种不同的是( )
| A. | HClO | B. | SO2 | C. | O3 | D. | H2O2 |
11.下列离子方程式正确的是( )
| A. | 醋酸与氢氧化钠溶液反应:OH-+H+═H2O | |
| B. | 氯气与水反应:Cl2+H2O?Cl-+HClO+H+ | |
| C. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| D. | 氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-═BaSO4↓ |
8.pH相同的CH3COOH、HCl和H2SO4溶液,分别用蒸馏水稀释到原来的X、Y、Z倍,稀释后三种溶液的pH仍然相同,则X、Y、Z的关系是( )
| A. | X=Y=Z | B. | X=Y<Z | C. | X>Y=Z | D. | X<Y=Z |
9.下列说法正确的是( )
| A. | 用分液漏斗分离除去溴苯中混入的溴 | |
| B. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| C. | 石油的裂解是化学变化,而石油的分馏和煤的干馏是物理变化 | |
| D. | 结构简式为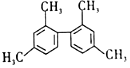 的分子中至少有11个碳原子处于同一平面上 的分子中至少有11个碳原子处于同一平面上 |