题目内容
14.检验制得的HCl气体中混有少量Cl2的方法是( )| A. | 观察气体的颜色 | B. | 用干燥的蓝色石蕊试纸 | ||
| C. | 用硝酸银溶液 | D. | 用湿润的淀粉碘化钾试纸 |
分析 HCl含少量氯气时,颜色不明显,且氯气可氧化KI生成碘单质,淀粉遇碘变蓝,以此来检验.
解答 解:A.杂质很少,观察颜色不能检验,故A不选;
B.氯气不能使干燥的蓝色石蕊试纸褪色,不能检验,故B不选;
C.HCl、氯气均与硝酸银反应生成AgCl沉淀,不能鉴别,故C不选;
D.氯气与KI反应碘,而HCl不能,用湿润的淀粉碘化钾试纸可检验,故D选;
故选D.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意氯气的性质及检验方法,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列有关实验装置及实验方案的设计不正确的是( )
| 选项 | A | B | C | D |
| 实验装置 | 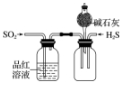 | 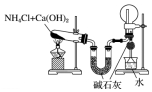 | 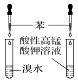 | 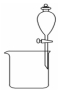 |
| 实验设计 | 探究SO2的氧化性和漂白性 | 实验室制氨气并收集干燥的氨气 | 验证苯中是否有碳碳双键 | 用乙醇提取溴水中的Br2 |
| A. | A | B. | B | C. | C | D. | D |
14.下列说法错误的是( )
| A. | 红陶中体现红色的成分是氧化铁,氧化铁属于碱性氧化物 | |
| B. | 丝绸的主要成分是蛋白质,蛋白质是天然高分子化合物 | |
| C. | 黑火药爆炸时,碳、硫两元素被氧化 | |
| D. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应 |
2.下列关于液氯和氯水的叙述中正确的是( )
| A. | 液氯较氯水的漂白作用更强 | B. | 液氯与氯水均有酸性 | ||
| C. | 液氯是纯净物,氯水是混合物 | D. | 液氯是无色的,氯水呈黄绿色 |
9.下列关于化学键的叙述正确的是( )
| A. | 全部由非金属元素组成的化合物中可含离子键 | |
| B. | H2O中所有原子都满足八电子稳定状态 | |
| C. | 两种元素构成的化合物可以含有非极性共价键 | |
| D. | CH4中所有的电子都参与形成共价键 |
19.下列说法正确的是( )
| A. | SO2通入BaCl2溶液中无现象,加入氨水后得到BaSO4沉淀 | |
| B. | SO2通入酸性KMnO4溶液中,溶液褪色,体现SO2的漂白性 | |
| C. | SO2通入紫色石蕊试液中,溶液变红色 | |
| D. | 等物质的量的SO2和Cl2通入水中,溶液的漂白性增强 |
6.检验CO2气体中是否有SO2,应采用的方法是,将气体( )
| A. | 通入澄清的石灰水 | |
| B. | 通入品红溶液 | |
| C. | 依次通过澄清石灰水和酸性KMnO4溶液 | |
| D. | 依次通过小苏打溶液和澄清石灰水 |
3.下列反应的离子方程式书写正确的是( )
| A. | 4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ | |
| B. | 硫酸氢钠溶液与氢氧化钡溶液混合显中性:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| C. | 稀硝酸中加入过量的铁粉:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| D. | 向AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
4.反应2A(g)?2B(g)+E(g)△H>0,达到平衡时,要使正反应速率降低,且B的物质的量增大,应采取的措施是( )
| A. | 加压 | B. | 增大体积 | C. | 减少A的浓度 | D. | 降温 |