题目内容
一定温度时,反应2HI(g)?H2(g)+I2(g);△H>0 达到平衡,要使混合气体颜色加深,可采用的方法是( )
| A、减小压强 |
| B、缩小体积 |
| C、降低温度 |
| D、增大H2的浓度 |
考点:化学平衡的影响因素
专题:
分析:要使混合气体的颜色加深,应使c(I2)增大,可使平衡向正反应方向移动,缩小容器的体积、升高温度等.
A、减小压强平衡不移动,但体积增大,c(I2)减小,混合气体的颜色变浅;
B、缩小体积,压强增大,平衡不移动,c(I2)增大,混合气体的颜色变深;
C、该反应正反应是吸热反应,降低温度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅;
D、增大氢气的浓度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅.
A、减小压强平衡不移动,但体积增大,c(I2)减小,混合气体的颜色变浅;
B、缩小体积,压强增大,平衡不移动,c(I2)增大,混合气体的颜色变深;
C、该反应正反应是吸热反应,降低温度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅;
D、增大氢气的浓度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅.
解答:
解:A、减小压强平衡不移动,但体积增大,c(I2)减小,混合气体的颜色变浅,故A错误;
B、缩小体积,压强增大,平衡不移动,c(I2)增大,混合气体的颜色变深,故B正确;
C、该反应正反应是吸热反应,降低温度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅,故C错误;
D、增大氢气的浓度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅,故D错误;
故选B.
B、缩小体积,压强增大,平衡不移动,c(I2)增大,混合气体的颜色变深,故B正确;
C、该反应正反应是吸热反应,降低温度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅,故C错误;
D、增大氢气的浓度,平衡向逆反应移动,c(I2)减小,混合气体的颜色变浅,故D错误;
故选B.
点评:本题考查影响化学平衡的因素,难度不大,注意把握从平衡移动的角度使c(I2)增大的措施.

练习册系列答案
相关题目
有A、B两种原子,A原子的第三电子层比B原子的第三电子层少3个电子,B原子的第二电子层电子数恰好为A原子第二电子层电子数的2倍.A和B分别是( )
| A、硅原子和钠原子 |
| B、硼原子和氦原子 |
| C、氯原子和碳原子 |
| D、碳原子和铝原子 |
固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:根据上述实验,以下说法正确的是( )
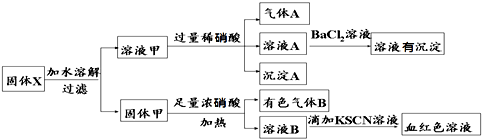

| A、气体A一定只是NO |
| B、由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液中含有K2SO3 |
| C、若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D、溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |
从柑桔中炼制出有机物 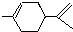 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )
 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )| A、分子式为C10H16 |
| B、常温下为液态,难溶于水 |
| C、属于芳香烃 |
| D、1mol该物质与1molHCl加成所得产物有四种 |
下列实验装置图所示的实验操作,能达到相应的实验目的是( )
A、 分离沸点相差较大液体混合物 |
B、 除去CO气体中的CO2气体 |
C、 向容量瓶中转移液体 |
D、 分离互不相溶的两种液体 |
在某容器中,C+H2O(g)?CO+H2反应达到平衡,在温度、体积不变的情况下,向容器中充入一定量H2,当建立新平衡时( )
| A、CO、H2的浓度都比原平衡时的要小 |
| B、CO、H2的浓度都比原平衡时的要大 |
| C、H2、H2O(g)的浓度都比原平衡时的要大 |
| D、CO、H2O(g)的浓度都比原平衡时的要大 |
下列四种物质的溶液,其中一种与其它三种能发生离子反应,这种物质是( )
| A、H2SO4 |
| B、KOH |
| C、BaCl2 |
| D、Na2CO3 |