题目内容
4g NaOH溶解在水中,要使Na+的离子数与水分子数之比为1:100,则需要水的物质的量为 mol,其溶液中有 mol OH-,中和这些OH-,需要 mol H+和 g H2SO4.
考点:物质的量的相关计算
专题:计算题
分析:每100个水分子中含有1个Na+,即100mol水中含有1molNaOH,也就是:100H2O~1molNaOH根据这个关系式解题.
解答:
解:因为每100个水分子中含有1个Na+,即100mol水中含有1molNaOH,也就是:
100H2O~1molNaOH
100 40
n(H2O) 4
所以n(H2O)=
=10mol
n(OH-)=n(NaOH)=
=0.1mol,
因为2OH-~H2SO4
2mol 98g
0.1mol 4.9g
需要的H+和OH-的物质的量相等,故n(H+)=n(OH-)=0.1mol.
故答案为:10;0.1;0.1;4.9.
100H2O~1molNaOH
100 40
n(H2O) 4
所以n(H2O)=
| 100×4 |
| 40 |
n(OH-)=n(NaOH)=
| 4g |
| 40g/mol |
因为2OH-~H2SO4
2mol 98g
0.1mol 4.9g
需要的H+和OH-的物质的量相等,故n(H+)=n(OH-)=0.1mol.
故答案为:10;0.1;0.1;4.9.
点评:本题考查化学方程式的有关计算,学生要找已知物质与要求物之间的关系即可,难度不大,注意基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
图象是一种简洁表示化学变化过程的方法,下列相关反应的图象中错误的是( )
A、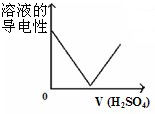 将一定量稀硫酸滴入到同浓度的Ba(OH)2溶液中 将一定量稀硫酸滴入到同浓度的Ba(OH)2溶液中 |
B、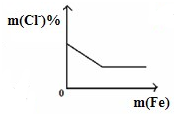 将铁粉加入到一定量FeCl3溶液中 将铁粉加入到一定量FeCl3溶液中 |
C、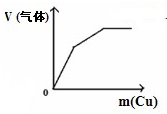 将铜粉加入到一定量浓硝酸中 将铜粉加入到一定量浓硝酸中 |
D、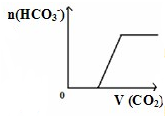 将二氧化碳通入到一定量漂粉精溶液中 将二氧化碳通入到一定量漂粉精溶液中 |
64g铜与一定浓度的硝酸反应,铜完全溶解,生成NO和NO2(不考虑生成N2O4)混合气体33.6L(所有气体体积均在标准状况下测得).下列说法正确的是( )
| A、产生的NO在标准状况下的体积为28L |
| B、参加反应的硝酸的物质的量为1.5mol |
| C、NO和NO2的物质的量之比为1:5 |
| D、若生成的气体完全被水吸收,需要标准状况下O2的体积为 22.4L |
 元素周期表是指导我们系统学习化学的重要工具.下表是元素周期表的一部分:
元素周期表是指导我们系统学习化学的重要工具.下表是元素周期表的一部分: