题目内容
11. 乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x值.通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO${\;}_{4}^{-}$+5H2C2O4+6H+═=2Mn2++10CO2↑+8H2O学习小组的同学设计了滴定的方法测定x值.
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x值.通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO${\;}_{4}^{-}$+5H2C2O4+6H+═=2Mn2++10CO2↑+8H2O学习小组的同学设计了滴定的方法测定x值.①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.100 0mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00mL.
(1)滴定时,KMnO4标准液装在如图中的甲(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志可以是当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点.
(3)通过上述数据,求得x=2.若滴定终点时俯视滴定管刻度,则由此测得的x值会偏大(填“偏大”、“偏小”或“不变”,下同).
分析 (1)因为酸高锰酸钾溶液具有强氧化性,腐蚀橡皮管;
(2)根据KMnO4溶液自身的颜色作为指示剂判断滴定终点时,再滴加KMnO4溶液时,溶液将由无色变为紫色.
(3)由题给化学方程式及数据计算出1.260g纯草酸晶体中含H2C2O4的物质的量,然后求出1.260g 纯草酸晶体中含H2O的物质的量,根据H2O的物质的量和纯草酸晶体的物质的量的关系求出x;若滴定终点时俯视滴定管读数,则所得消耗酸性KMnO4溶液的体积偏小,由此所得n(H2C2O4)偏小,则n(H2O)偏大,x偏大.
解答 解:(1)酸高锰酸钾溶液具有强氧化性,腐蚀橡皮管,所以用酸式滴定管,
故答案为:甲;
(2)因KMnO4溶液自身的颜色作为指示剂判断滴定终点时,再滴加KnO4溶液时,溶液将由无色变为紫色,
故答案为:当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;
(3)2MnO4-+5H2C2O4 +6H+═2Mn2++10CO2↑+8H2O
2 5
0.1000mol/L×0.01L 0.0025mol
25.00mL待测液中含有0.0025molH2C2O4,100.00mL待测液中含有0.01molH2C2O4,0.01molH2C2O4的质量为0.01mol
×90g/mol=0.9g,所以1.260g纯草酸晶体中水的物质的量为1.260g-0.9g=0.36g,其物质的量为0.02mol,则x=2,
若滴定终点时俯视滴定管读数,则所得消耗酸性KMnO4溶液的体积偏小,由此所得n(H2C2O4)偏小,则n(H2O)偏大,x偏大,
故答案为:2;偏大.
点评 本题考查了滴定操作,操作时要规范,分析误差时要看是否影响标准体积的用量,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案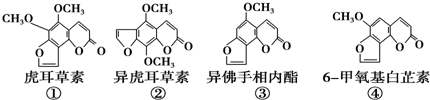
下列推断正确的是( )
| A. | ②、③互为同系物 | |
| B. | ①、③各1mol与足量氢氧化钠溶液反应时均消耗3molNaOH | |
| C. | 等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者少 | |
| D. | ③、④互为同分异构体,它们各1mol均能与5molH2加成 |
| A. | 放电时,锂铝合金作负极,Li+向负极移动 | |
| B. | 充电时,阴极的电极反应式为:Fe+2Li2S-4e-=4Li++FeS2 | |
| C. | 该电池可用LiCl水溶液作电解质溶液 | |
| D. | 以Al作阳极,FeS为阴极,LiCl-KCl低共熔混合物为电解质进行电解,可以制得FeS2 |
完成下列填空:
(1)上述反应涉及的第三周期元素中,离子半径最小的是Al3+;Cl原子与Si原子可构成有5个原子核的分子,其分子的空间构型为正四面体.
(2)用最详尽描述核外电子运动状态的方式,表示氧离子核外电子的运动状态
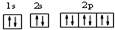 .
.(3)Na和O2反应形成Na2O和Na2O2的混合物,阴阳离子的个数比为1:2;NaAlSi3O8改写成氧化物形式是Na2O•Al2O3•6SiO2.
(4)某兴趣小组为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量分数)与温度的关系,进行实验(保持其它条件不变),获得如下数据:
时间/h 熔出率 温度 | 1.5 | 2.5 | 3.0 | 3.5 | 4.0 |
| 800℃ | 0.054 | 0.091 | 0.127 | 0.149 | 0.165 |
| 830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 |
| 860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 |
| 950℃ | 0.669 | 0.711 | 0.713 | 0.714 | 0.714 |
(5)Na(l)+KCl(l)?NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,该方法可行的原因是根据勒夏特列原理,将钾蒸气分离出来(降低了产物的浓度),化学平衡向正反应方向移动.
(6)铝可用于冶炼难熔金属,利用铝的亲氧性,还可用于制取耐高温的金属陶瓷.例如将铝粉、石墨和二氧化钛按一定比例混合均匀,涂在金属表面上,然后在高温下煅烧,可在金属表面形成耐高温的涂层TiC,该反应的化学方程式为4Al+3TiO2+3C $\frac{\underline{\;高温\;}}{\;}$2Al2O3+3TiC.

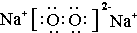
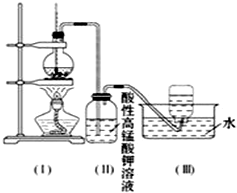 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后溶液中有黑色现象出现.过一段时间后,经硫酸酸化的高锰酸钾溶液褪色.经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O.
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后溶液中有黑色现象出现.过一段时间后,经硫酸酸化的高锰酸钾溶液褪色.经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O.
