题目内容
19.制备干燥的氨气所需的药品是( )| A. | NH4Cl溶液,NaOH溶液 | B. | 浓NaOH溶液,NH4Cl晶体,浓H2SO4 | ||
| C. | 浓氨水,浓硫酸 | D. | NH4Cl固体,消石灰,碱石灰 |
分析 实验室用氯化铵和消石灰加热反应制备氨气,氨气为碱性气体,易溶于水,干燥氨气应用碱性或中性干燥剂.
解答 解:A.氨气易溶于水,不能用溶液制备氨气,故A错误;
B.氨气为碱性气体,易于浓硫酸反应,不能用浓硫酸干燥,故B错误;
C.氨气为碱性气体,不能用浓硫酸干燥,故C错误;
D.实验室用氯化铵和消石灰反应制备氨气,氨气为碱性气体,可用碱石灰干燥,故D正确.
故选D.
点评 本题考查氨气的制备和干燥,侧重于氨气性质的考查,较为基础,难度不大,实验室制备氨气可用氯化铵和消石灰反应,也可用浓氨水和碱石灰或氢氧化钠固体制备.

练习册系列答案
相关题目
9.控制城市污染源的方法有( )
| A. | 戴上呼吸面具 | B. | 把垃圾倒入河水 | C. | 开发新能源 | D. | 大量使用塑料袋 |
10.某有机物的分子式为C5H10O,它能够发生银镜反应和加成反应,若将它与H2加成,所得产物结构简式可能是( )
| A. | (CH3)2CHCH(CH3)OH | B. | (CH3CH2)2CHOH | C. | CH3CH2C(CH3)2OH | D. | CH3(CH2)3CH2OH |
7.H2S在O2中不完全燃烧生成S和H2O.下列说法正确的是( )
| A. | 氧元素的单质存在同素异形体 | B. | 微粒半径:O2->S2- | ||
| C. | 还原性:H2S<H2O | D. | 该反应中化学能全部转化为热能 |
11.锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水.当生成2mol硝酸锌时,被还原的硝酸的物质的量为( )
| A. | 1mol | B. | 0.5mol | C. | 0.25 mol | D. | 0.125 mol |
8.下列物质中的杂质(括号内为杂质)的检验、除杂试剂或方法正确的是( )
| 选项 | 物质及杂质 | 检验 | 除杂试剂或方法 |
| A | I2(Cl2) | 湿润的淀粉-KI试纸 | NaI溶液 |
| B | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
| C | CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和Na2CO3溶液 |
| D | NO(NO2) | 观察颜色或湿润的淀粉-KI试纸 | 水 |
| A. | A | B. | B | C. | C | D. | D |
17.下列说法正确的是( )
| A. | 热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的数据 | |
| B. | 升高温度或加入催化剂,不能改变化学反应的反应热 | |
| C. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| D. | 物质发生化学变化不一定伴随着能量变化 |
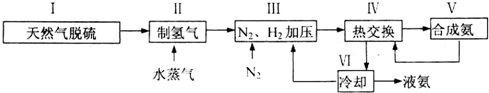
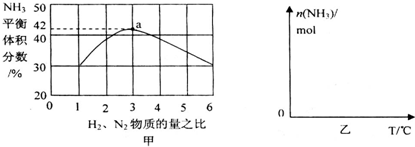
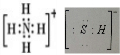 ,写出再生反应的化学方程式:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S;NH3的沸点高于H2S,是因为NH3分子之间存在着一种叫分子间作用的作用力.
,写出再生反应的化学方程式:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S;NH3的沸点高于H2S,是因为NH3分子之间存在着一种叫分子间作用的作用力.