题目内容
10.某有机物的分子式为C5H10O,它能够发生银镜反应和加成反应,若将它与H2加成,所得产物结构简式可能是( )| A. | (CH3)2CHCH(CH3)OH | B. | (CH3CH2)2CHOH | C. | CH3CH2C(CH3)2OH | D. | CH3(CH2)3CH2OH |
分析 有机物的分子式为C5H10O,它能发生银镜反应和加成反应,所以该有机物为醛,醛跟H2的加成反应是发生在 上,使之转化为-CH2OH,得到的醇羟基必定在碳链的端点碳上,即伯醇,以此解答该题.
上,使之转化为-CH2OH,得到的醇羟基必定在碳链的端点碳上,即伯醇,以此解答该题.
解答 解:该有机物能发生银镜反应和加成反应,所以该有机物为醛,其可能的同分异构体有:CH3CH2CH2CH2-CHO、CH3CH(CH3)CH2CHO、CH3CH2CH(CH3)CHO、(CH3)3CCHO,醛跟H2的加成反应是发生在 上,使之转化为-CH2OH,得到的醇羟基必定在碳链的端点碳上,即伯醇,
上,使之转化为-CH2OH,得到的醇羟基必定在碳链的端点碳上,即伯醇,
A、B、C羟基连接的C不满足端点碳的条件,只有D符合条件,
故选D.
点评 本题考查有机物分子式的确定,为高考常见题型,题目难度不大,注意把握有机物的结构和官能团的性质,明确醇的催化氧化特点为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
20. 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
(1)COCl2的空间构型为平面三角形;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式分解. A.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsCl+ICl B.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsI+Cl2
(3)根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘.
(4)下列分子既不存在s-p σ键,也不存在p-p π键的是D.
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中中心氯原子的杂化轨道类型为sp3杂化,写出与CN-互为等电子体的分子:N2或 CO(写出1个).
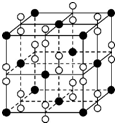
(6)钙在氧气中燃烧时得到一种钙的氧化物固体,其结构如图所示.由此可判断该钙的氧化物的化学式为CaO2.已知该氧化物的密度是ρ g•cm-3,则晶胞中离得最近的两个钙离子间的距离为$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{72×4}{ρN{\;}_{A}}}$ cm(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA).
 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.(1)COCl2的空间构型为平面三角形;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式分解. A.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsCl+ICl B.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsI+Cl2
(3)根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘.
| 氟 | 氧 | 溴 | 碘 | |
| 第一电离能 (kJ/mol) | 1 681 | 1 251 | 1 140 | 1 008 |
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中中心氯原子的杂化轨道类型为sp3杂化,写出与CN-互为等电子体的分子:N2或 CO(写出1个).
(6)钙在氧气中燃烧时得到一种钙的氧化物固体,其结构如图所示.由此可判断该钙的氧化物的化学式为CaO2.已知该氧化物的密度是ρ g•cm-3,则晶胞中离得最近的两个钙离子间的距离为$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{72×4}{ρN{\;}_{A}}}$ cm(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA).
1.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.其中Z所处的周期序数与族序数相等.下列说法不正确的是( )
| X | Y | Q | ||
| Z | W |
| A. | 形成简单离子的半径大小顺序:r(W)>r(Z)>r(Y) | |
| B. | 最简单气态氢化物的热稳定性:Y>X | |
| C. | Q的氢化物的水溶液可用于蚀刻玻璃 | |
| D. | X、Z的最高价氧化物均可与NaOH溶液反应 |
5.向FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤沉淀,然后在空气中灼烧沉淀,最终得到的固体物质是( )
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)3 | D. | Fe3O4 |
15.对于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0 的化学反应下列叙述不正确的是( )
| A. |  反应过程中能量关系可用图表示 | |
| B. | 该反应为自发反应 | |
| C. | 若将该反应设计成原电池则锌为负极 | |
| D. | 若将其设计为原电池,当有32.5g锌溶解时,正极放出气体为11.2L |
2.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 不法商家制取的“地沟油”具有固定的熔沸点 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 在家可用食醋代替CO2来增强漂白粉的漂白性 |
19.制备干燥的氨气所需的药品是( )
| A. | NH4Cl溶液,NaOH溶液 | B. | 浓NaOH溶液,NH4Cl晶体,浓H2SO4 | ||
| C. | 浓氨水,浓硫酸 | D. | NH4Cl固体,消石灰,碱石灰 |