题目内容
下列溶液中有关物质的物质的量浓度的大小关系正确的是( )
| A、常温下,在pH=8的HCOONa溶液中:c(Na+)-c(HCOO-)=9.9×10-7mol/L |
| B、Na2CO3溶液中:c(Na+)=2c(CO32-)+2c(HCO3-) |
| C、室温下,由pH=1的CH3COOH溶液与pH=13的NaOH溶液等体积混合,溶液中离子浓度大小的顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3?H2O; c(NH4+)由大到小的顺序是:②>①>③>④ |
考点:离子浓度大小的比较
专题:
分析:A.溶液中遵循电荷守恒,根据电荷守恒进行计算;
B.根据碳酸钠溶液中的物料守恒进行分析;
C.常温下,pH=1的醋酸溶液中浓度大于pH=13的氢氧化钠,二者等体积混合时醋酸过量,溶液呈酸性;
D.①铝离子水解抑制铵根离子的水解;②铵根离子水解;③弱碱电离,且电离的程度很弱;④醋酸根离子水解促进铵根离子水解.
B.根据碳酸钠溶液中的物料守恒进行分析;
C.常温下,pH=1的醋酸溶液中浓度大于pH=13的氢氧化钠,二者等体积混合时醋酸过量,溶液呈酸性;
D.①铝离子水解抑制铵根离子的水解;②铵根离子水解;③弱碱电离,且电离的程度很弱;④醋酸根离子水解促进铵根离子水解.
解答:
解:A.溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(HCOO-)+c(OH-),所以c(Na+)-c(HCOO-)=c(OH-)-c(H+)=10-7 mol/L-10-8 mol/L=9.9×10-7mol/L,故A正确;
B.碳酸钠溶液中存在物料守恒,根据物料守恒得:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B错误;
C.常温下,pH=1的醋酸溶液中氢离子浓度为0.1mol/L,醋酸浓度大于0.1mol/L;而pH=13的氢氧化钠溶液的浓度为0.1mol/L,二者等体积混合时醋酸过量,醋酸电离程度大于醋酸根离子水解程度,所以溶液呈酸性,则c(H+)>c(OH-),正确的浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D.同浓度的下列溶液:①NH4Al(SO4)2②NH4Cl③CH3COONH4④NH3?H2O,因①中铝离子水解抑制铵根离子的水解;②中铵根离子水解;③醋酸根离子水解促进铵根离子水解,④弱碱电离,且电离的程度很弱,则c(NH4+)由大到小的顺序是:①>②>③>④,故D错误;
故选A.
B.碳酸钠溶液中存在物料守恒,根据物料守恒得:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B错误;
C.常温下,pH=1的醋酸溶液中氢离子浓度为0.1mol/L,醋酸浓度大于0.1mol/L;而pH=13的氢氧化钠溶液的浓度为0.1mol/L,二者等体积混合时醋酸过量,醋酸电离程度大于醋酸根离子水解程度,所以溶液呈酸性,则c(H+)>c(OH-),正确的浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D.同浓度的下列溶液:①NH4Al(SO4)2②NH4Cl③CH3COONH4④NH3?H2O,因①中铝离子水解抑制铵根离子的水解;②中铵根离子水解;③醋酸根离子水解促进铵根离子水解,④弱碱电离,且电离的程度很弱,则c(NH4+)由大到小的顺序是:①>②>③>④,故D错误;
故选A.
点评:本题考查离子浓度大小的比较,题目难度较大,熟悉酸的强弱与盐的水解的关系,电荷守恒、水解与电离的程度及相互影响是解答本题的关键,试题培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
一定温度和压强不变的条件下,发生可逆反应:A(g)+3B(g)?4C(g)下列叙述能作为该反应达到平衡状态的标志的是( )
①混合气体的平均摩尔质量不再变化
②v(A):v(B):v(C)=1:3:4
③A、B、C的浓度不再变化
④C的体积分数不再变化
⑤A、B、C的分子数之比为1:3:4
⑥混合气体的密度不再变化
⑦单位时间消耗amolA,同时生成3amolB.
①混合气体的平均摩尔质量不再变化
②v(A):v(B):v(C)=1:3:4
③A、B、C的浓度不再变化
④C的体积分数不再变化
⑤A、B、C的分子数之比为1:3:4
⑥混合气体的密度不再变化
⑦单位时间消耗amolA,同时生成3amolB.
| A、②③④⑤⑥⑦ | B、③④⑦ |
| C、②③④⑦ | D、①③⑤⑥⑦ |
下列关于有机化合物组成与结构判断正确的是( )
| A、有机物一定都含碳、氢元素 |
| B、分子中含有羟基的化合物属于醇类 |
| C、分子式相同,各元素质量分数也相同的物质是同种物质 |
| D、有机物分子中,氢原子数不一定都是偶数 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、在0.1 mol?L-1 NaHCO3溶液中:c(CO3 2- )>c(H2CO3) |
| B、在0.1 mol?L-1 Na2CO3溶液中:c(OH- )=c(HCO3- )+c(H2CO3)+c(H+ ) |
| C、某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子,该溶液可能由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| D、c(NH4+)相等的(NH4)2SO4溶液、(NH4)2 Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2 Fe(SO4)2]<c[(NH4)2 SO4]<c(NH4Cl) |
下列物质中,不属于合金的是( )
| A、碳素钢 | B、黄铜 | C、钢铁 | D、金箔 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、澄清透明溶液中:Cl-、NO3-、Cu2+、NH4+ |
| B、水电离产生的c(OH-)=1×10-11mol/L的溶液:Cu2+、SO42-、NO3-、Cl- |
| C、中性溶液中:Fe3+、Al3+、NO3-、SO42- |
| D、能使苯酚变紫色的溶液:K+、Mg2+、S2-、SO42- |
反应2NO+2CO
N2+2CO2可应用于汽车尾气的净化.下列判断正确的是( )
| ||
| △ |
| A、该反应是置换反应 |
| B、该反应是复分解反应 |
| C、碳元素化合价降低 |
| D、该反应是氧化还原反应 |

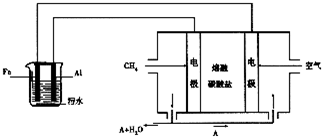 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置如图所示: