题目内容
根据下列实验现象,所得结论正确的是( )


| 实验 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 先生成蓝色沉淀,后产生白色沉淀 | 溶度积常数:Mg(OH)2<Cu(OH)2 |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.活动性为Al>Fe>Cu;
B.不能证明氧化性Br2>I2;
C.先生成溶度积小的沉淀;
D.比较非金属性应为最高价氧化物的水化物的酸性.
B.不能证明氧化性Br2>I2;
C.先生成溶度积小的沉淀;
D.比较非金属性应为最高价氧化物的水化物的酸性.
解答:
解:A.左烧杯中铁表面有气泡,说明活动性Al>Fe,右边烧杯中铜表面有气泡,说明活动性Fe>Cu,则活动性为Al>Fe>Cu,故A正确;
B.因生成的Br2中含有Cl2,则不能证明氧化性Br2>I2,故B错误;
C.先生成溶度积小的沉淀,应先生成氢氧化镁沉淀,故C错误;
D.比较非金属性应为最高价氧化物的水化物的酸性,不能用盐酸,并且盐酸易挥发,生成的二氧化碳中混有HCl,不能证明非金属性C>Si,故D错误.
故选A.
B.因生成的Br2中含有Cl2,则不能证明氧化性Br2>I2,故B错误;
C.先生成溶度积小的沉淀,应先生成氢氧化镁沉淀,故C错误;
D.比较非金属性应为最高价氧化物的水化物的酸性,不能用盐酸,并且盐酸易挥发,生成的二氧化碳中混有HCl,不能证明非金属性C>Si,故D错误.
故选A.
点评:本题考查实验方案的评价,题目难度中等,易错点是能正确把握比较物质性质的角度.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
证明氨水是弱碱的事实是( )
| A、氨水与硫酸发生中和反应 |
| B、氨水能使紫色石蕊试液变蓝 |
| C、0.1 mol/L的NH4Cl溶液的pH值为5.1 |
| D、浓氨水易挥发 |
对于反应A2+3B2?2C来说,以下化学反应速率的表示中,反应速率最快的是( )
| A、v(B2)=0.08 mol?(L?s)-1 |
| B、v(A2)=0.04 mol?(L?s)-1 |
| C、v(C)=3.6 mol?(L?min)-1 |
| D、v(B2)=5.4 mol?(L?min)-1 |
能正确表示下列化学反应的离子方程式是( )
| A、用氢氧化钠溶液吸收少量二氧化硫:2OH-+SO2═SO32-+H2O |
| B、金属铝溶于盐酸中:Al+2H+═Al3++H2↑ |
| C、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
| D、碳酸镁溶于硝酸中:CO32-+2H+═H2O+CO2↑ |
在下列物质 ①NaHCO3 ②MgCl2 ③Na2CO3 ④(NH4)2CO3中,与盐酸和氢氧化钙溶液均可反应的是( )
| A、③④ | B、①③④ | C、② | D、① |
在无色透明的强酸性溶液中,能大量共存的离子组是( )
| A、K+、Na+、NO3-、MnO4- |
| B、Mg2+、Na+、Cl-、SO42- |
| C、K+、Cu2+、Br-、S2- |
| D、NH4+、Al3+、I-、NO3- |

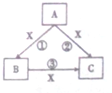 在化学反应中,反应物相同时,因反应条件不同或反应物的量不同产物可能不同,已知A,B,C,X均为中学化学中的常见物质,在常温下它们有如图转化关系(部分产物已略去)回答下列问题
在化学反应中,反应物相同时,因反应条件不同或反应物的量不同产物可能不同,已知A,B,C,X均为中学化学中的常见物质,在常温下它们有如图转化关系(部分产物已略去)回答下列问题