题目内容
9.同温同压下,相同体积的CO2和NO两种气体,两者的物质的量的比为1:1,密度之比为22:15,质子数之比为22:15.分析 根据阿伏加德罗定律可知,同温同压下同体积的CO2和NO的物质的量相同,根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$结合物质的构成计算该题.
解答 解:由n=$\frac{V}{{V}_{m}}$可知,相同体积的CO2和NO两种气体,两者的物质的量的比为1:1;
1molCO2的质量为1mol×44g/mol=44g,1molNO的质量为1mol×30g/mol=30g,质量之比为44:30=22:15;
因CO2和NO的体积相同,则密度之比等于质量之比,为22:15;
CO2含有22个质子,NO含有15个质子,则质子数之比为22:15,
故答案为:1:1;22:15;22:15.
点评 本题考查阿伏加德罗定律及其推论,涉及物质的量的有关计算,题目难度不大,注意相关计算公式的运用,侧重于学生的分析能力和计算能力的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.有关溶度积Ksp的说法正确的是( )
| A. | Ksp的数值只与温度有关 | |
| B. | Ksp的数值只与难溶电解质的性质和温度有关 | |
| C. | Ksp的大小与沉淀量有多少和溶液中离子浓度的大小有关 | |
| D. | Ksp的数值越大,电解质在水中的溶解能力越强 |
4.下列实验操作中正确的是( )
| A. | 用规格为10mL的量筒量取6.20mL的液体 | |
| B. | 称量氢氧化钠固体的质量时,将称量物放在滤纸上,并置于托盘天平的左盘,砝码放在托盘天平的右盘 | |
| C. | 利用蒸馏可除去液态混合物中沸点不同的易挥发、难挥发或不挥发的杂质 | |
| D. | 用四氯化碳萃取碘水中的碘,充分静置后紫红色液体在上层 |
14.向KOH溶液中通入8.96L(标准状况)氯气恰好完全反应生成三种含氯盐:0.6molKCl、0.1molKClO和X.则X是( )
| A. | 0.1molKClO4 | B. | 0.1molKClO3 | C. | 0.1molKClO2 | D. | 0.2molKClO |
1.工业上用某矿渣(主要成分是Cu2O,少量杂质是Al2O3、Fe2O3和SiO2)提取铜的操作流程如下:
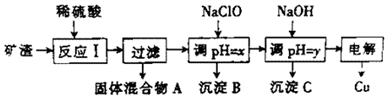
已知:①Cu2O+2H+═Cu+Cu2++H2O ②某些金属氢氧化物开始测沉淀和完全沉淀时的pH
(1)反应I中,与铁元素有关反应的离子方程式为Fe2O3+6H+═2Fe3++3H2O、2Fe3++Cu═2Fe2++Cu2+.
(2)y的数值范围是5.2≤pH<5.4.
(3)以上步骤中的NaOH可以用AC代替(填字母)
A.CuO B.NH4Cl C.Cu(OH)2
(4)电解过程中,阳极产物可能为Cl2、O2.
(5)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为2Fe2++5ClO-+5H2O=2Fe(OH)3+Cl-+4HClO.

已知:①Cu2O+2H+═Cu+Cu2++H2O ②某些金属氢氧化物开始测沉淀和完全沉淀时的pH
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
| 沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
(2)y的数值范围是5.2≤pH<5.4.
(3)以上步骤中的NaOH可以用AC代替(填字母)
A.CuO B.NH4Cl C.Cu(OH)2
(4)电解过程中,阳极产物可能为Cl2、O2.
(5)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为2Fe2++5ClO-+5H2O=2Fe(OH)3+Cl-+4HClO.
18.已知448℃时反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)的平衡常数是$\frac{1}{7}$,则H2(g)+I2(g)?2HI(g)在该温度下的平衡常数是( )
| A. | $\frac{1}{14}$ | B. | 14 | C. | $\frac{1}{49}$ | D. | 49 |
4.向密闭容器中充入1.0mol CO和2.0mol H2O(g)发生反应:CO+H2O(g)?CO2+H2.当反应达平衡时,CO的转化率为α.若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达平衡时CO的转化率小于α的是( )
| A. | 0.5molCO+2.0molH2O(g)+1.0molCO2+1.0mol H2 | |
| B. | 1.0molCO+2.0molH2O(g)+0.5molHe | |
| C. | 1.0molCO+1.0molH2O(g)+1.0molCO2+1.0mol H2 | |
| D. | 0.5molCO+1.5molH2O(g)+0.4molCO2+0.4mol H2 |
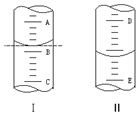 ①如图Ⅰ表示10mL量筒中液面的位置.A与B,B与C刻度间相差1mL,如果刻度A为6,量筒中液体的体积是5.2 mL.
①如图Ⅰ表示10mL量筒中液面的位置.A与B,B与C刻度间相差1mL,如果刻度A为6,量筒中液体的体积是5.2 mL.