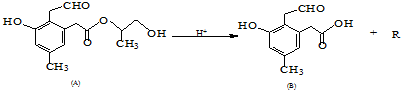
题目内容
下列化学实验事实及其结论都正确的是( )
| 实验事实 | 结 论 | |
| A | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| B | HCl与Na2CO3溶液反应生成CO2 | 可用饱和Na2CO3溶液除去CO2中的少量HCl |
| C | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| D | SO2通入KMnO4酸性溶液中,红色褪去 | SO2有漂白性 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,常见金属元素的单质及其化合物的综合应用
专题:实验评价题,元素及其化合物
分析:A.常温下铁在浓硫酸中发生钝化现象生成氧化物薄膜阻止反应进行;
B.碳酸钠溶液可以和二氧化碳水反应生成碳酸氢钠;
C.铝箔熔化但不滴落,原因是表面生成氧化铝膜,熔点较高;
D.二氧化硫与酸性高锰酸钾发生氧化还原反应.
B.碳酸钠溶液可以和二氧化碳水反应生成碳酸氢钠;
C.铝箔熔化但不滴落,原因是表面生成氧化铝膜,熔点较高;
D.二氧化硫与酸性高锰酸钾发生氧化还原反应.
解答:
解:A.常温下铁在浓硫酸中发生钝化反应生成致密氧化物薄膜阻止反应进行,常温下铜不与浓硫酸反应不溶于浓硫酸,故A错误;
B.饱和碳酸钠溶液可以吸收氯化氢,也可以吸收二氧化碳生成碳酸氢钠,故B错误;
C.铝箔熔化但不滴落,原因是表面生成氧化铝膜,熔点较高,即熔点:氧化铝>铝,故C正确;
D.二氧化硫具有还原性,可与酸性高锰酸钾发生氧化还原反应,故D错误.
故选C.
B.饱和碳酸钠溶液可以吸收氯化氢,也可以吸收二氧化碳生成碳酸氢钠,故B错误;
C.铝箔熔化但不滴落,原因是表面生成氧化铝膜,熔点较高,即熔点:氧化铝>铝,故C正确;
D.二氧化硫具有还原性,可与酸性高锰酸钾发生氧化还原反应,故D错误.
故选C.
点评:本题考查化学实验方案的设计,涉及物质性质的考查,侧重点较为基础,题目难度不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
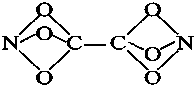 某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )
某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )| A、该分子的分子式为CNO3 |
| B、分子中既含极性键又含非极性键 |
| C、C、N的化合价分别为+4、+3 |
| D、该物质为高分子化合物 |
实验室中需要0.2mol?L-1的NaOH溶液65mL,配制该溶液时应选用的容量瓶的规格和称取的NaOH质量分别是( )
| A、65 mL,0.52 g |
| B、70 mL,0.56 g |
| C、100 mL,0.52 g |
| D、100 mL,0.8 g |
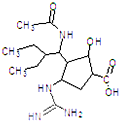 2013年4月5日国家食品药品监督管理局批准了抗H7N9流感新药帕拉米韦氯化钠注射液,帕拉米韦结构如图所示.下列有关说法正确的是( )
2013年4月5日国家食品药品监督管理局批准了抗H7N9流感新药帕拉米韦氯化钠注射液,帕拉米韦结构如图所示.下列有关说法正确的是( )| A、该分子式为C15H28N4O4 |
| B、帕拉米韦能发生取代、加成、消去和氧化反应 |
| C、该分子为难溶于水的药物,遇FeCl3溶液显紫色 |
| D、该分子中含有4种官能团 |
关于反应K35ClO3+6H37Cl═KCl+3Cl2↑+3H2O的有关叙述中,正确的是( )
| A、KCl中含有35Cl |
| B、生成物Cl2的相对分子质量为73.3 |
| C、该反应转移的电子数为6e- |
| D、氧化剂和还原剂的物质的量之比为1:6 |
 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是次外层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是次外层电子数的3倍,下列说法正确的是( )| A、原子半径:X<Z<W |
| B、非金属性:Y>Z |
| C、最高化合价:X<Y |
| D、最高价氧化物对应水化物的酸性:W>Z |
下列说法不正确的是( )
| A、(NH4)2SO4和CuSO4溶液都能使蛋白质沉淀析出 |
B、苯酚与甲醛在酸性条件下生成酚醛树脂的结构简式为 |
| C、醋酸和硬脂酸互为同系物,C6H14和C9H20也一定互为同系物 |
D、叶酸的结构为 ,它可以发生酯化、水解、加成等反应 ,它可以发生酯化、水解、加成等反应 |