题目内容
三氟化硼分子的空间构型是 ;三溴化硼、三氯化硼分子结构与三氟化硼相似,如果把B-X键都当作单键考虑来计算键长,理论值与实测键长结果如表.硼卤键长实测值比计算值要短得多,可能的原因是 .
| 键长/(pm) | B-F | B-Cl | B-Br |
| 计算值 | 152 | 187 | 199 |
| 实测值 | 130 | 175 | 187 |
考点:判断简单分子或离子的构型,键能、键长、键角及其应用
专题:化学键与晶体结构
分析:根据鲍林(Pauling)的杂化轨道理论:价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=
×(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,根据价层电子对互斥理论确定其空间构型;sp3杂化,无孤电子对数,空间构型都是正四面体形;有一对孤电子对,空间构型是三角锥型;有两对孤电子,所以分子空间构型为V形;sp2杂化,无孤电子对数,空间构型是平面三角形;sp杂化,无孤电子对数,空间构型都是直线形;硼卤键长实测值比计算值要短得多,可能的原因是B与X原子间还有π键形成.
| 1 |
| 2 |
解答:
解:BF3中B形成3个σ键,孤对电子数为
×(3-3×1)=0,为sp2杂化,立体构型为平面正三角形;硼卤键长实测值比计算值要短得多,可能的原因是B-X键具有一定程度的双键性质,在B原子上有一个空的2p轨道从三个卤素原子上的任何一个已经充满电子的对称性相同的p轨道接受一对电子形成了p-pπ键,
故答案为:平面三角形;B与X原子间还有π键形成.
| 1 |
| 2 |
故答案为:平面三角形;B与X原子间还有π键形成.
点评:本题考查BF3分子的构型判断以及有关三氯化硼分子结构知识,题目难度中等,注意判断中心原子的价层电子对以及孤对电子数的判断.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
用NA表示阿伏加德罗常数.下列叙述正确的是( )
| A、25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B、标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C、在0℃、1.01KPa下,22.4L的NO气体与11.2L的O2混合,气体分子数为NA |
| D、在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA |
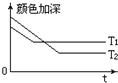 (1)反应A+B?2C,其中A为有色气态物质,其混合物颜色深浅与反应时间,温度(T)之间的关系如图所示(B、C均为无色物质):
(1)反应A+B?2C,其中A为有色气态物质,其混合物颜色深浅与反应时间,温度(T)之间的关系如图所示(B、C均为无色物质):