题目内容
9.(1)检验食盐中是否加碘,可利用如下反应:1KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O
①将上述氧化还原反应的化学方程式配平.
②该反应中,氧化剂和还原剂的物质的量之比为1:5.
③如果反应中转移0.2mol电子,则生成I2的物质的量为0.12 mol.
(2)在弱酸性条件下,向FeSO4溶液中加入KMnO4溶液可得到一种有特殊颜色的难溶性碱及一种难溶性氧化物,写出相应离子方程式:3Fe2++7H2O+MnO4-=MnO2+3Fe(OH)3↓+5H+.
分析 (1)分析反应元素化合价变化,依据氧化还原反应化合价升降数相等结合原子个数守恒配平方程式;所含元素化合价降低的反应物为氧化剂,所含元素化合价升高的反应物为还原剂;结合元素化合价的变化计算电子转移数目;
(2)高锰酸钾具有强的氧化性,二价铁离子具有强的还原性,向FeSO4溶液中加入KMnO4溶液可得到一种有特殊颜色的难溶性碱及一种难溶性氧化物,依据氧化还原反应规律可知产物为氢氧化铁沉淀和二氧化锰固体,结合原子个数守恒写出方程式.
解答 解:(1)①方程式中:碘酸钾中碘元素由+5价降为碘单质中0价碘,碘化钾中-1价碘升高为碘单质中0价碘,要使化合价升降数目相等,则碘酸钾系数为1,碘化钾系数为5,依据原子个数守恒反应方程式为:KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O;
故答案为:1;5;3;3;3;
②KIO3为氧化剂,KI为还原剂,由方程式可知氧化剂和还原剂的物质的量之比为1:5,
故答案为:1:5;
③依据方程式:KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O,可知生成3mol碘单质,转移电子数5mol,则转移0.2mol电子,则生成I2的物质的量0.12mol;
故答案为:0.12mol;
(2)高锰酸钾具有强的氧化性,二价铁离子具有强的还原性,向FeSO4溶液中加入KMnO4溶液可得到一种有特殊颜色的难溶性碱及一种难溶性氧化物,依据氧化还原反应规律可知产物为氢氧化铁沉淀和二氧化锰固体,二价铁离子被氧化生成三价铁离子,化合价升高1,高锰酸根中的+7价锰降为二氧化锰中+4价,降3价,依据化合价升级数目相等则二价铁离子系数为3,高锰酸根离子系数为1,结合原子个数守恒,可知反应方程式:3Fe2++7H2O+MnO4-=MnO2+3Fe(OH)3↓+5H+;
故答案为:3Fe2++7H2O+MnO4-=MnO2+3Fe(OH)3↓+5H+.
点评 本题考查了氧化还原反应方程式的书写,明确氧化还原反应中化合价升降数目相等、原子个数守恒规律是解题关键,题目难度不大.

 ABC考王全优卷系列答案
ABC考王全优卷系列答案| A. | pH=10的NaOH和CH3COONa溶液中,水的电离程度 | |
| B. | 25℃与80℃纯水的pH | |
| C. | 将pH=3的醋酸和盐酸分别稀释100倍后溶液的pH | |
| D. | 相同温度下,10mL0.1mol•L-1的醋酸与100mL0.01mol•L-1的醋酸中的H+物质的量 |
 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质.
某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质.(一)他们先把铜粉放在空气中灼烧,在与稀HNO3反应制取硝酸铜.
(1)如果直接用铜屑与HNO3反应来制取硝酸铜,可能导致的两个不利因素是生成等物质的量的硝酸铜,消耗硝酸原料多、且产生污染物氮氧化物.
(2)实验中铜粉应该放在坩埚(填“蒸发皿”、“坩埚”或“烧杯”)中灼烧.欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序分别蒸发浓缩、冷却结晶、过滤.
(二)为了探究Cu(NO3)2热稳定性,探究小组用下图中的装置进行实验.(图中铁架台、铁夹和加热设备均略去)
往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在右试管中收集到无色气体.
(1)红棕色气体是NO2.
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意先把导气管移出水面,然后熄灭火焰.
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有O2 ,写出该反应的化学方程式2Cu(NO3)2═2CuO+4NO2↑+02↑.
(三)为了探究Cu(NO3)2在酸性条件下跟铁单质的反应.他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质.
(1)反应中最先起氧化作用的是HNO3;
(2)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验.请在答题卡上按下表格式补充写出实验操作步骤、预期现象与结论.
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色,不能(填“能”或“不能”确定产物中铁元素的价态. |
步骤2:取少量溶液,滴加酸性KMn4溶液 | 若KMnO4溶液的紫红色褪去或变浅,则说明产物中含+2价铁元素,若KMnO4溶液不褪色或不变浅,则说明产物中不含+2价铁元素 |
| 步骤3:另取少量溶液,滴加KSCN溶液 | 若溶液变为血红色,说明产物中含+3价的铁元素;若溶液颜色无明显变化,则说明产物中不含+3价的铁元素. |
| A. | 浓的强酸和稀的强碱溶液反应 | B. | 浓的弱酸和稀的强碱溶液反应 | ||
| C. | 等pH值的强酸和弱碱溶液反应 | D. | 生成一种强酸弱碱盐 |
| A. | 25℃时,1L 0.1mol/L的CH3COOH溶液中的H+数为0.1NA | |
| B. | 常温常压下,30g葡萄糖含有的氧原子数为NA | |
| C. | 0.1mol/L的AlCl3溶液中含有的氯离子数为0.3NA | |
| D. | 16 g甲烷分子中含有共价键的数目为2NA |
| 溶液 | 甲+乙 | 乙+丙 | 丙+丁 | 甲+丁 |
| 现象 | 无明显现象 | 白色沉淀 | 白色沉淀 | 无色气体 |
| A. | HCl、BaCl2、H2SO4、Na2CO3 | B. | H2SO4、HCl、BaCl2、Na2CO3 | ||
| C. | HCl、H2SO4、BaCl2、Na2CO3 | D. | H2SO4、Na2CO3、HCl、BaCl2 |
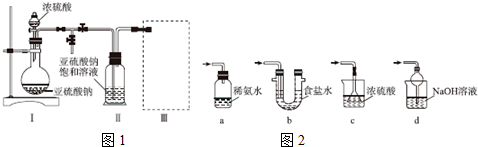



 ;I中所含化学键类型离子键、共价键,气体D所含元素在周期表中的位置第三周期ⅤⅡA族
;I中所含化学键类型离子键、共价键,气体D所含元素在周期表中的位置第三周期ⅤⅡA族