题目内容
下列叙述中,正确的是( )
| A、硫酸的摩尔质量是98 |
| B、1mol氧的质量等于16g |
| C、摩尔是一个基本物理量 |
| D、以克为单位时,12g12C所含的原子数为阿伏伽德罗常数 |
考点:物质的量的单位--摩尔,摩尔质量
专题:
分析:A.摩尔质量是有单位的,摩尔质量的单位为g/mol;
B.1mol氧,没有指明是氧气分子还是氧原子;
C.摩尔是物质的量的单位,物质的量为基本物理量;
D.根据阿伏伽德罗常数的标准进行判断.
B.1mol氧,没有指明是氧气分子还是氧原子;
C.摩尔是物质的量的单位,物质的量为基本物理量;
D.根据阿伏伽德罗常数的标准进行判断.
解答:
解:A.硫酸的摩尔质量为98g/mol,98为硫酸的相对分子质量,故A错误;
B.使用物质的量必须指明粒子的具体名称,如1mol氧气、1mol氧原子,故B错误;
C.物质的量是国际单位制中基本物理量,摩尔是物质的量的单位,故C错误;
D.以克为单位时,12g12C的物质的量为1mol,所含的原子数为阿伏伽德罗常数,故D正确;
故选D.
B.使用物质的量必须指明粒子的具体名称,如1mol氧气、1mol氧原子,故B错误;
C.物质的量是国际单位制中基本物理量,摩尔是物质的量的单位,故C错误;
D.以克为单位时,12g12C的物质的量为1mol,所含的原子数为阿伏伽德罗常数,故D正确;
故选D.
点评:本题考查了物质的量与摩尔、摩尔质量与相对分子质量等物理量之间关系,题目难度不大,试题侧重基础知识的考查,明确物质的量、摩尔质量、相反的总质量等概念为解答关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列反应达到平衡后,加压或升温,平衡都向正反应方向移动的是( )
| A、2NO2(g)?N2O4(g)△H<0 |
| B、3O2(g)?2O3(g)△H>0 |
| C、H2(g)+I2(g)?2HI(g)△H<0 |
| D、NH4HCO3(s)?NH3(g)+H2O(g)+CO2(g)△H>0 |
NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、25℃时,Ph=12的NaOH溶液中含有OH-的数目为0.01NA |
| B、1L 0.25mol.L-1醋酸溶液中含CH3COOH分子数为0.25NA |
| C、7.8gNa2O2中阴阳离子总数为0.4NA |
| D、标准状况下,2.24L氧气与氮气的混合气体所含分子数为0.1NA |
对于反应MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑,下列说法错误的是( )
| ||
| A、该反应是氧化还原反应 |
| B、MnO2发生还原反应 |
| C、HCl是还原剂 |
| D、若生成7.1 g Cl2,则转移0.1 mol电子 |
下列四种物质“水解”时,其反应物和产物之间化合价发生明显变化的是( )
| A、Na2O2的水解产物是NaOH和H2O2 |
| B、PCl3的水解产物是PH3和HClO |
| C、Mg3N2的水解产物是Mg(OH)2和NH3 |
| D、SiCl4的水解产物是H4SiO4与HCl |
下列说法正确的是( )
| A、金属元素的原子最外层电子数越少,则该元素的金属性越强 |
| B、同周期元素原子半径和离子半径从左到右均依次减小 |
| C、第三周期非金属氧化物对应水化物的酸性从左到右依次增强 |
| D、第ⅦA族元素气态氢化物的还原性从上到下依次增强 |
下列化学用语表达正确的是( )
A、硝基苯的结构简式: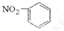 | ||
B、NH4Cl的电子式: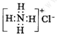 | ||
C、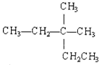 的名称为:3,3二甲基戍烷 的名称为:3,3二甲基戍烷 | ||
D、具有16个质子、16个种子和18个电子的微粒一定是
|