题目内容
13.如图为锌铜原电池装置示意图,下列说法不正确的是( )
| A. | 电子由Zn极流向Cu极 | B. | 此装置能将电能转变为化学能 | ||
| C. | 取出盐桥,电流表指针不再偏转 | D. | 该装置的总反应:Zn+Cu2+═Zn2++Cu |
分析 该装置是原电池,锌作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流向正极,以此解答.
解答 解:A.锌比铜活泼,形成原电池反应时,锌为负极,铜为正极,电子由Zn极流向Cu极,故A正确;
B.该装置为原电池,此装置能将化学能转变为电能,故B错误;
C.取出盐桥,不能形成闭合回路,没有电流,所以电流表指针不再偏转,故C正确;
D.该原电池的原理是Zn与硫酸铜的置换反应,则总反应:Zn+Cu2+═Zn2++Cu,故D正确;
故选B.
点评 本题考查原电池知识,为高考高频考点,侧重于学生的分析能力的考查,注意把握原电池的组成以及工作原理,能正确书写电极方程式,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
3.高温条件下,Al和Fe2O3反应生成Fe和Al2O3.下列说法正确的是( )
| A. |  该反应过程中的能量变化如图所示 | |
| B. | 该反应条件下,Al的还原性强于Fe | |
| C. | 反应中每生成1 mol Fe转移6×6.02×1023个电子 | |
| D. | 实验室进行该反应时常加入KClO3作催化剂 |
4.能正确表示下列反应的离子方程式的是( )
| A. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O?Cl2↑+H2↑+2OH- | |
| B. | 向氯化铝溶液中滴加少量Na2CO3溶液:2Al3++3CO32-?Al2(CO3)3↓ | |
| C. | 一定量明矾溶液中滴加Ba(OH)2溶液至沉淀的质量最大时:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O | |
| D. | FeCl3溶液与NaAlO2溶液混合:Fe3++3AlO2-?Fe(AlO2)3↓ |
1.下列实验的现象和所得结论均正确的是( )
| 选项 | 实验 | 现象 | 由现象所得结论 |
| A | 将Cl2通入品红溶液 | 品红褪色 | Cl2具有漂白性 |
| B | 向白色AgCl悬浊液中滴加0.1mol/LKI溶液 | 试管中白色沉淀转化为黄色沉淀. | Ksp(AgCl)>Ksp(AgI) |
| C | 将CO2通入CaCl2溶液中 | 无明显现象 | 非金属性:Cl>C |
| D | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| A. | A | B. | B | C. | C | D. | D |
18.在一定体积的1L密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
下列说法正确的是( )
| t/℃ | 700 | 800 | 830 | 1 000 |
| K | 0.6 | 0.9 | 1.0 | 1.7 |
| A. | 上述生成CO和H2O的反应为放热反应 | |
| B. | 加压、增大H2浓度和加入催化剂都能提高CO2的转化率 | |
| C. | 830℃达平衡后,再充入1.0 mol H2,K值增大,平衡正向移动 | |
| D. | 830℃时反应CO(g)+H2O(g)?CO2(g)+H2(g)的平衡常数为1 |
4.室温下,下列说法中错误的是( )
| A. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) | |
| B. | pH=5的下列溶液(①NH4Cl溶液②CH3COOH溶液;③稀盐酸)中由水电离出来的c(H+)水 ①>②>③ | |
| C. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) | |
| D. | pH相同的下列三种溶液(①CH3COONa、②NaHCO3、③NaClO)中的c(Na+):①>②>③ |
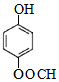
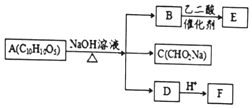 某芳香化合物A有如下转化:
某芳香化合物A有如下转化: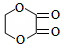 1mol F 最多消耗2mol NaOH.
1mol F 最多消耗2mol NaOH.