题目内容
15. S2Cl2是工业上常用的硫化剂,已知S2C12中硫元素显+1价,它不稳定,在水中易发生岐化反应,易溶于有机溶剂.实验室常用CS2与纯净的氯气制备S2C12.反应涉及到的几种物质的熔沸点如表:
S2Cl2是工业上常用的硫化剂,已知S2C12中硫元素显+1价,它不稳定,在水中易发生岐化反应,易溶于有机溶剂.实验室常用CS2与纯净的氯气制备S2C12.反应涉及到的几种物质的熔沸点如表:| 物质 | CS2 | Cl2 | CCl4 | S2C12 |
| 沸点/℃ | 47 | -34.6℃ | 77 | 137 |
| 熔点/℃ | -109 | -100.98℃ | -23 | -77 |
回答下列问题:
(1)装置中b玻璃仪器的名称为冷凝管;写出制备S2C12的化学方程式CS2+3Cl2$\stackrel{111-140℃}{→}$CCl4+S2Cl2.
(2)整套装置装配完毕后,首先进行的操作是气密性检查,再添加试剂.
(3)实验中盐酸试剂通常采用36.5%的浓盐酸,不用稀盐酸的理由是稀盐酸还原性弱,反应困难.装置A中反应的离子方程式是MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O.
(4)D中采用热水浴加热的原因是使CS2平稳汽化,避免产物S2Cl2汽化,反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏.
(5)实验过程中,若缺少C装置,则发现产品浑浊不清,出现该现象的原因化学方程式表示为2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.
(6)该实始装置设计存在缺陷,你的改进建议及改进目的是D和E之间应连接一个干燥装置,避免S2C12水解.
分析 制取原理是:显示二氧化锰和浓盐酸之间反应得到氯气,但是氯气中混油HCl和水,应该先用饱和食盐水除去HCl,再用浓硫酸干燥氯气,让氯气和二硫化碳在一定温度下发生反应:CS2+3Cl2$\stackrel{111-140℃}{→}$CCl4+S2Cl2,为了使CS2平稳汽化,避免产物S2Cl2汽化,采用热水浴加热的方法,根据S2Cl2的熔沸点数据,采用冷凝回流的办法将之收集即可试验中的氯气要进行尾气处理,可以用氢氧化钠来吸收;
(1)根据仪器的结构和作用判断仪器的名称;CS2与纯净的氯气反应生成S2C12和CCl4,结合原子守恒写出此反应的化学方程式;
(2)反应是封闭体系,有气体的制备及尾气的处理,可结合实验的基本操作考虑;
(3)二氧化锰和稀盐酸之间几乎不反应;依据实验室制备氯气的方法分析,用二氧化锰和浓盐酸加热反应生成氯气;
(4)氯气中的HCl以及水杂质应该除去,根据表中物质的沸点高低可以进行物质的分离;
(5)根据题干信息:S2Cl2在水中易发生岐化反应来书写反应方程式;
(6)S2Cl2在水中易发生岐化反应,应防止有水蒸气进入反应容器中.
解答 解:制取原理是:显示二氧化锰和浓盐酸之间反应得到氯气,但是氯气中混油HCl和水,应该先用饱和食盐水除去HCl,再用浓硫酸干燥氯气,让氯气和二硫化碳在一定温度下发生反应:CS2+3Cl2$\stackrel{111-140℃}{→}$CCl4+S2Cl2,为了使CS2平稳汽化,避免产物S2Cl2汽化,采用热水浴加热的方法,根据S2Cl2的熔沸点数据,采用冷凝回流的办法将之收集即可试验中的氯气要进行尾气处理,可以用氢氧化钠来吸收;
(1)装置中b起到导气和冷凝回流双重作用,其玻璃仪器的名称为冷凝管;制备S2C12的化学方程式为CS2+3Cl2$\stackrel{111-140℃}{→}$CCl4+S2Cl2;
答案为:冷凝管;CS2+3Cl2$\stackrel{111-140℃}{→}$CCl4+S2Cl2;
(2)A装置仪器装配时,整套装置装配完毕后,应先进行气密性的检查,再添加试剂,
故答案为:气密性检查;
(3)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸,因为稀盐酸还原性弱,反应困难;用固液加热的方法制Cl2,常用浓盐酸和二氧化锰反应制取,反应离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:稀盐酸还原性弱,反应困难;MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O;
(4)根据表中物质的沸点高低,为了使CS2平稳汽化,避免产物S2Cl2汽化,可以采用水浴加热的方法,结束后从锥形瓶内混合物中分离出S2Cl2的方法是蒸馏,控制温度在
137℃,故答案为:使CS2平稳汽化,避免产物S2Cl2汽化;蒸馏;
(5)S2Cl2与水反应,有无色刺激性气味气体产生,并有黄色沉淀生成,无色刺激性气味气体除氯化氢外,依据氧化还原反应的元素化合价变化守恒推断,化合价降低的生成黄色沉淀为单质硫,化合价升高的生成二氧化硫气体,依据原子守恒、电子守恒写出化学方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑,
故答案为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑;
(6)为避免S2Cl2遇水蒸气水解,在D和E之间应连接一个干燥装置,防止水蒸气进入制备S2Cl2的锥形瓶中,
故答案为:D和E之间应连接一个干燥装置,避免S2C12水解.
点评 本题考查了氯气实验室制备方法,杂质气体除杂的装置选择和试剂选择,题干信息的应用分析,电子式书写,化学方程式书写方法,混合物分离的方法判断,题目难度中等.

 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,c(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,c(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
(2)如图中表示NO2的浓度变化曲线是曲线a.
(3)用NO表示从0~2s内该反应的平均速率v=0.03mol/(L•s).
(4)v(NO):v(O2)=2:1.
(5)达到平衡状态时O2的转化率为70%.
| A. |  图中,Zn-MnO2干电池放电时,MnO2被氧化 | |
| B. |  图中,电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 | |
| C. |  图中,在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl7-形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl7- | |
| D. |  图中,K分别与M、N连接,均可保护Fe电极,连接M时为“牺牲阳极的阴极保护法” |
 工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H.如表所列数据是该反应在不同温度下的化学平衡常数(K).
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H.如表所列数据是该反应在不同温度下的化学平衡常数(K).| 温度 | 250℃ | 300℃ | 350℃ |
| K/L2•mol-2 | 2.041 | 0.270 | 0.012 |
(2)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,4min达到平衡时测得c(CO)=0.2mol•L-1,此时的温度为250℃,则反应速率v(H2)=0.32 mol•L-1•min-1.
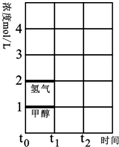
(3)T℃时,在时间t0时刻,合成甲醇反应CO(g)+2H2(g)?CH3OH(g)达到平衡,若在t1时刻将容器的体积缩小w为原来的$\frac{1}{2}$,假定在t2时刻后又达到新的平衡,请在图中用曲线表示在t1~t2阶段氢气、甲醇物质的量浓度随时间变化的趋势示意图(其它条件不变,曲线上必须标明氢气、甲醇).
(4)如果用CH3OH和空气作燃料电池,用KOH作电解质溶液,请写出该燃料电池的负极的电极反应式CH3OH-6e-+8OH-=CO32-+6H2O.
| A. | △H单位中的每摩尔指的既不是每摩尔C4H10,也不是其他反应物或生成物,而是每摩尔反应 | |
| B. | 该反应的△H与各物质的状态有关,与化学计量数也有关 | |
| C. | 该式的含义为:25℃、101 kPa下,2 mol C4H10气体完全燃烧生成CO2和液态水时放出热量5 800 kJ | |
| D. | 该反应为丁烷燃烧的热化学方程式,由此可知丁烷的燃烧热为5 800 kJ/mol |
| A. | 若降低温度,可以加快反应速率 | |
| B. | 增大O2浓度可以增大反应速率 | |
| C. | 随着反应的进行,正反应速率逐渐减小,最后变为0 | |
| D. | 达到化学平衡状态时,SO2和SO3的浓度一定相等 |
 主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题: .
. )的方法中,原子经济性最好的是(反应均在一定条件下进行)( )
)的方法中,原子经济性最好的是(反应均在一定条件下进行)( )


