题目内容
 如图是制取溴苯的装置,试回答:
如图是制取溴苯的装置,试回答:(1)装置A中发生反应的化学方程式是
(2)装置B是吸收瓶,内盛CCl4液体,B的作用是
(3)装置C中看到的现象是
(4)C中的离子方程式为
(5)实验完毕后将A管中的液体倒在盛有冷水的烧杯中,烧杯中液体的
考点:苯的性质
专题:有机物的化学性质及推断
分析:(1)苯与液溴在铁做催化剂条件下发生取代反应生成溴苯;
(2)溴易挥发,易溶于四氯化碳;
(3)溴化氢与硝酸银反应生成浅黄色溴化银沉淀;
(4)溴化氢与硝酸银反应生成溴化银和硝酸;
(5)根据溴苯的物理性质进行分析.
(2)溴易挥发,易溶于四氯化碳;
(3)溴化氢与硝酸银反应生成浅黄色溴化银沉淀;
(4)溴化氢与硝酸银反应生成溴化银和硝酸;
(5)根据溴苯的物理性质进行分析.
解答:
解:(1)苯与液溴在铁做催化剂条件下发生取代反应化学方程式为: ;
;
故答案为: ;
;
(2)溴易挥发,易溶于四氯化碳,用四氯化碳吸收挥发出来的溴;
故答案为:吸收挥发出来的溴;
(3)溴化氢与硝酸银反应生成浅黄色溴化银沉淀;
故答案为:产生浅黄色沉淀;
(4)溴化氢与硝酸银反应生成溴化银和硝酸,反应的方程式为:Ag++Br-=AgBr↓;
故答案为:Ag++Br-=AgBr↓;
(5)实验完毕后将A管中的液体倒在盛有冷水的烧杯中,烧杯中液体的下层为溴苯层,这说明溴苯不溶于水,密度大于水;
故答案为:溴苯难溶于水 密度大于水.
 ;
;故答案为:
 ;
;(2)溴易挥发,易溶于四氯化碳,用四氯化碳吸收挥发出来的溴;
故答案为:吸收挥发出来的溴;
(3)溴化氢与硝酸银反应生成浅黄色溴化银沉淀;
故答案为:产生浅黄色沉淀;
(4)溴化氢与硝酸银反应生成溴化银和硝酸,反应的方程式为:Ag++Br-=AgBr↓;
故答案为:Ag++Br-=AgBr↓;
(5)实验完毕后将A管中的液体倒在盛有冷水的烧杯中,烧杯中液体的下层为溴苯层,这说明溴苯不溶于水,密度大于水;
故答案为:溴苯难溶于水 密度大于水.
点评:本题考查了苯的性质,题目难度不大,熟悉苯的结构和性质是解题的关键.

练习册系列答案
相关题目
元素X的原子比元素Y的原子多一层电子,X、Y的单质都能与水激烈反应放出气体,所生成的两种气体混合点燃,会发生爆炸,X、Y形成的离子都与氖原子有相同的电子层结构,则X、Y可能是( )
| A、Na和Cl | B、K和F |
| C、Na和F | D、Ca和Cl |
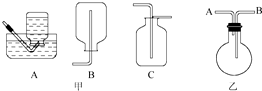
用下列实验装置进行相应实验,能达到实验目的是( )


| A、图③将硫酸铜溶液蒸干,制备蓝矾 |
| B、图④除去HCl中含有的少量Cl2 |
| C、图①完成“喷泉”实验 |
| D、图②制取并收集干燥纯净的NH3 |
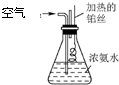 在50mL锥形瓶中盛有20mL浓氨水,向氨水中鼓入空气并迅速将烧红的铂丝伸入瓶中并接近浓氨水的液面.试回答:
在50mL锥形瓶中盛有20mL浓氨水,向氨水中鼓入空气并迅速将烧红的铂丝伸入瓶中并接近浓氨水的液面.试回答:

 实验室通过加热氯化铵和消石灰来制取氨气.
实验室通过加热氯化铵和消石灰来制取氨气.