题目内容
如图表示4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.
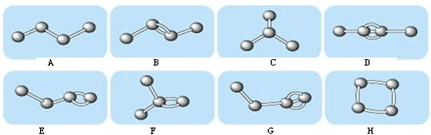
(1)图中属于烷烃的是 (填编号).
(2)在如图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成 和 ;不仅可以形成碳链,还可以形成碳环.
(3)图中,B与 互为同分异构体(填编号).

(1)图中属于烷烃的是
(2)在如图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成
(3)图中,B与
考点:球棍模型与比例模型,有机化合物中碳的成键特征,同分异构现象和同分异构体
专题:有机物分子组成通式的应用规律
分析:(1)烷烃分子中,碳原子和其他原子均以单键成键;
(2)碳原子之间成键方式具有多样性,可以成碳链可以成碳环,可以形成双键、单键、三键;
(3)分子式相同而结构不同的有机化合物互为同分异构体.
(2)碳原子之间成键方式具有多样性,可以成碳链可以成碳环,可以形成双键、单键、三键;
(3)分子式相同而结构不同的有机化合物互为同分异构体.
解答:
解:(1)根据图示的球棍模型可以看出,只有A、C中碳原子和其他原子以共价单键结合,属于烷烃,
故答案为:AC;
(2)碳原子之间成键方式具有多样性,碳原子与碳原子之间不仅可以形成共价单键,还可以形成双键、单键,不仅可以形成碳链还可以形成碳环,
故答案为:碳碳双键;碳碳叁键;
(3)B为2-丁烯,分子式为C4H8,E、F、H的分子式都为C4H8,且它们的结构不同,所以B与E、F、H互为同分异构体,
故答案为:E、F、H.
故答案为:AC;
(2)碳原子之间成键方式具有多样性,碳原子与碳原子之间不仅可以形成共价单键,还可以形成双键、单键,不仅可以形成碳链还可以形成碳环,
故答案为:碳碳双键;碳碳叁键;
(3)B为2-丁烯,分子式为C4H8,E、F、H的分子式都为C4H8,且它们的结构不同,所以B与E、F、H互为同分异构体,
故答案为:E、F、H.
点评:本题考查了球棍模型、有机化合物中碳的成键特征、同分异构体等知识,题目难度不大,注意掌握对信息的理解运用、读图方法,本题能够加深对同分异构体概念的理解,培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
能正确表示下列反应的离子方程式的是( )
A、硫酸溶液与氢氧化钡溶液混合:2H++S
| ||||
B、NaCO3溶液水解:HCO
| ||||
C、NaOH溶液中加入铝片:Al+2OH-═Al
| ||||
D、NH4HCO3溶液与足量烧碱溶液混合:HC
|
下列各组离子在溶液中能大量共存的是( )
| A、Ba2+、Cl-、SO42-、K+ |
| B、Fe3+、OH-、Na+、Br- |
| C、Ca2+、HCO3-、Cl-、K+ |
| D、Ag+、NO3-、Cl-、K+ |
下列表示对应化学反应的离子方程式正确的是( )
A、过氧化钠固体与水反应:2O
| ||||
B、碳酸钠的水解反应:CO
| ||||
C、AlCl3溶液中滴加浓氨水至过量:Al3++4NH3?H2O=Al
| ||||
D、铁溶于稀硝酸,溶液变黄:Fe+4H++NO
|
设NA是阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L乙醇中含有的氧原子数为NA |
| B、6.4g的S2和S8混合物中,含硫原子总数为0.2 NA |
| C、1L 0.1mol/L氯化铁溶液中,含有0.1NA个Fe3+ |
| D、25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为0.2NA |
下列离子方程式书写正确的是( )
| A、向NaOH溶液中通入足量SO2:SO2+2OH-=SO32-+H2O |
| B、碳酸钡中加入稀硫酸:BaCO3+2H+=Ba2++CO2↑+H2O |
| C、SiO2溶于NaOH溶液:SiO2+2OH-=SiO32-+H2O |
| D、Fe2O3溶于过量的氢碘酸:Fe2O3+6H+=2Fe3++3H2O |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol Na2O2与水反应转移电子数为NA |
| B、0.1 mol FeCl3水解制成胶体,所碍胶体粒子数为0.1NA |
| C、标准状况下,22 4 L水中含有水分子数为NA |
| D、1 L 0.1 mol?L-1乙酸溶液中H+数为0.1NA |