题目内容
2.下列用离子方程式解释正确的是( )| A. | 用氢氟酸在玻璃上镌刻图案:4I++SiO2═H2O+Si4+ | |
| B. | 向Cu2+、Fe3+混合液中加入CuO除去Fe3+;3H2O+3CuO+2Fe3+═2Fe(OH)3+3Cu2+ | |
| C. | 亚硫酸氢钠溶液显酸性:HSO3-═H++SO32- | |
| D. | 用盐酸与碳酸钠反应证明氯的非金属性强与炭:2H++CO32-═CO2↑+H2O |
分析 A.氢氟酸为弱电解质,应保留化学式;
B.依据盐类水解平衡移动影响因素解答;
C.亚硫酸氢根离子为多元弱酸的酸式根离子,部分电离,用可逆号;
D.盐酸不是氯元素的最高价氧化物对应的水化物,无法证明非金属性强弱.
解答 解:A.用氢氟酸在玻璃上镌刻图案,离子方程式:4HF+SiO2═2H2O+SiF4,故A错误;
B.三价铁离子为弱碱阳离子,存在水解平衡生成氢离子和氢氧化铁,氢离子与氧化铜反应消耗氢离子促进三价铁离子水解,离子方程式:3H2O+3CuO+2Fe3+═2Fe(OH)3+3Cu2+,故B正确;
C.亚硫酸氢钠溶液显酸性,离子方程式:HSO3-?H++SO32-,故C错误;
D.最高价含氧酸酸性越强,元素非金属性越强,氯化氢为无氧酸,不能用来判断非金属性强弱,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,熟悉离子方程式书写方法,明确盐类水解影响因素是解题关键,题目难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
12.常温下,KSP[Mn(OH)2]=2.0×10-13.实验室制氯气的废液中含c(Mn2+)=0.1mol•L-1,向该溶液中滴加稀氢氧化钠溶液至Mn2+完全沉淀的最小pH等于( )
| A. | 8+$\frac{1}{2}$ lg2 | B. | 9+lg2 | C. | 10+$\frac{1}{2}$ lg2 | D. | 11+2lg2 |
13.常温下,在含CH3COOH和CH3COONa均为0.1mol/L的溶液中,测得pH<7,则下列说法中正确的是( )
| A. | c(CH3COO-)<c(Na+) | B. | c(CH3COOH)+c(CH3COO-)=0.2mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COO-)>c(Na+) |
10.一定温度下可逆反应N2(g)+3H2(g)?2NH3(g)达平衡的标志是:(分别用V表示正反应速率,V╯表示逆反应速率)( )
| A. | V(N2)=V╯(NH3) | B. | V(N2)=3V(H2) | ||
| C. | V(H2)=3/2V╯(NH3) | D. | N2,H2,NH3的体积比为1:3:2 |
17.下列有关物质结构的表述正确的是( )
| A. | H2O2的电子式: | B. | CO2的比例模型: | ||
| C. | 14C的原子结构示意图: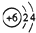 | D. | CCl4的结构式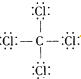 |
7.短周期主要素X、Y、Z、W,在周期表中的相对位置如图所示,下列说法正确的是( )
| X | Y |
| Z | W |
| A. | 若HmXOn为强酸,则Y的氢化物溶于水显酸性(m、n均为正整数) | |
| B. | 若W(OH)n为两性氢氧化物,则Z(OH)m为强碱(m、n均为正整数) | |
| C. | 若气体XHn不溶于水,则HmWOn为强酸(m、n、a均为正整数) | |
| D. | 若HmZOn为强酸,则气体HnY易溶于水(m、n、a均为正整数) |
14.化学与人类生活密切相关,下列与化学有关的说法正确的是( )
| A. | “海水淡化”可以解决“淡水供应危机”,加入明矾可以使海水淡化 | |
| B. | 化学药品着火,都要立即用水或泡沫灭火器灭火 | |
| C. | 可溶性铜盐有毒,但在生命体中,铜是一种不可缺少的微量元素 | |
| D. | 石油催化裂化的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
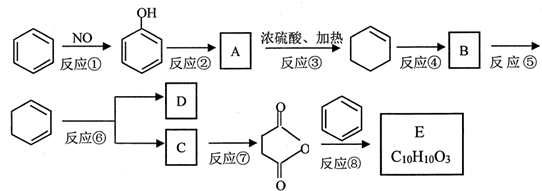
 +(CH3CO)2O→
+(CH3CO)2O→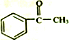 +CH3COOH
+CH3COOH ;B
;B .
. 直接制取
直接制取 ,原因是苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷.
,原因是苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷.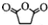 +
+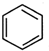 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$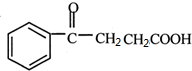 .
.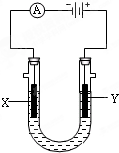 电解原理在化学工业中有广泛应用.
电解原理在化学工业中有广泛应用.