题目内容
13.工业冶炼钛的第一步反应为:TiO2(s)+2C(s)+2Cl2 $\stackrel{高温}{→}$TiCl4(g)+2CO.下列关于该反应的说法正确的是( )| A. | TiCl4既是氧化产物又是还原产物 | |
| B. | 氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 当转移电子数目为0.2NA时,气体体积增大1.12L | |
| D. | 当有26g固体参加反应时,转移电子数目为NA. |
分析 TiO2+2C+2Cl2→TiCl4+2CO中,C元素的化合价升高,Cl元素的化合价降低,以此来解答.
解答 解:A.Ti、O元素的化合价不变,Cl元素的化合价降低,TiCl4是还原产物,故A错误;
B.氯气为氧化剂,C为还原剂,由反应可知,氧化剂与还原剂的物质的量之比为1:1,故B正确;
C.当转移电子数目为0.2NA时,消耗0.05molCl2,生成0.055mol气体,在标准状况下,气体体积增大1.12L,没有说明是标准状况下,故C错误;
D.不能确定固体中C和TiO2的质量关系,无法计算,故D错误;
故选B.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念和转移电子的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.油酸的结构简式是( )
| A. | CH2=CHCOOH | B. | C15H31COOH | C. | C17H33COOH | D. | C17H35COOH |
4.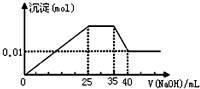 有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-,现取样逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.以下推测错误的是( )
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-,现取样逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.以下推测错误的是( )
 有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-,现取样逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.以下推测错误的是( )
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-,现取样逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.以下推测错误的是( )| A. | 原溶液一定不存在H+、Cu2+、CO32- | |
| B. | 不能确定原溶液是否含有K+、NO3- | |
| C. | 原溶液中n(Mg2+):n(Al3+):n(NH4+)=1:1:2 | |
| D. | 实验所加的NaOH溶液浓度为2mol/L |
1.常温下非固态的物质是( )
| A. | 软脂酸(C15H31COOH) | B. | 油酸(C17H33COOH) | ||
| C. | 草酸(HOOC-COOH) | D. | 氨基酸(H2N-CH2COOH) |
8.检验SO2气体中是否混有CO2的方法是( )
| A. | 先通过足量澄清石灰水,再通过足量品红溶液 | |
| B. | 先通过足量饱和NaHCO3溶液,再通过澄清石灰水 | |
| C. | 先通过足量NaOH溶液,再通过澄清石灰水 | |
| D. | 先通过足量酸性KMnO4溶液,再通过澄清石灰水 |
5.下列事实可以用同一原理解释的是( )
| A. | 乙烯使溴水、高锰酸钾溶液褪色 | |
| B. | 碘片、氯化铵晶体受热消失 | |
| C. | 二氧化硫和氯气使品红溶液褪色 | |
| D. | 乙醛、葡萄糖与银氨溶液水浴加热反应 |
3.下列关于自然界中氮循环示意图(如图)的说法错误的是( )

| A. | 氮元素只被氧化 | |
| B. | 豆科植物根瘤菌固氮属于自然固氮 | |
| C. | 其它元素也参与了氮循环 | |
| D. | 含氮无机物和含氮有机物可相互转化 |
 氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.
氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.