题目内容
如图是一个制取氯气并以氯气为原料进行某些反应的装置.(夹持和加热装置省略).

(1)写出图中仪器A的名称: .
(2)装置中x试剂为 ;装置中饱和食盐水的作用是 .
(3)装置③中发生反应的化学方程式为 .
(4)若将生成的C12通入淀粉碘化钾无色溶液中,可观察到溶液变成 色,反应的离子方程式为 .

(1)写出图中仪器A的名称:
(2)装置中x试剂为
(3)装置③中发生反应的化学方程式为
(4)若将生成的C12通入淀粉碘化钾无色溶液中,可观察到溶液变成
考点:氯气的实验室制法
专题:实验题
分析:(1)熟悉常见仪器,知道其名称;
(2)氯气有毒不能直接排放的空气中,可以用氢氧化钠溶液吸收氯气;从①中出来的氯气含有挥发的氯化氢气体杂质,可用饱和食盐水吸收;
(3)氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水;
(4)氯气的氧化性强于碘,能够氧化碘离子生成单质碘,碘与淀粉变蓝.
(2)氯气有毒不能直接排放的空气中,可以用氢氧化钠溶液吸收氯气;从①中出来的氯气含有挥发的氯化氢气体杂质,可用饱和食盐水吸收;
(3)氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水;
(4)氯气的氧化性强于碘,能够氧化碘离子生成单质碘,碘与淀粉变蓝.
解答:
解:(1)A的名称是:分液漏斗,故答案为:分液漏斗;
(2)氯气有毒不能直接排放的空气中,可以用氢氧化钠溶液吸收氯气;氯化氢易溶于水,可以用饱和食盐水吸收挥发的氯化氢;
故答案为:氢氧化钠溶液;除去Cl2中混有的HCl;
(3)氯气与氢氧化钙反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(4)氯气的氧化性强于碘,将生成的C12通入淀粉碘化钾无色溶液中,发生反应的离子方程式:Cl2+2I-=2Cl-+I2,碘与淀粉变蓝色,
故答案为:蓝;Cl2+2I-=2Cl-+I2.
(2)氯气有毒不能直接排放的空气中,可以用氢氧化钠溶液吸收氯气;氯化氢易溶于水,可以用饱和食盐水吸收挥发的氯化氢;
故答案为:氢氧化钠溶液;除去Cl2中混有的HCl;
(3)氯气与氢氧化钙反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(4)氯气的氧化性强于碘,将生成的C12通入淀粉碘化钾无色溶液中,发生反应的离子方程式:Cl2+2I-=2Cl-+I2,碘与淀粉变蓝色,
故答案为:蓝;Cl2+2I-=2Cl-+I2.
点评:本题考查了氯气的实验室制法及化学性质,难度不大,明确制备的原理和各个装置的作用是解题关键,氯气制备和性质检验是高考热点,注意知识的积累.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
下列关于有机化合物的叙述中正确的是( )
| A、KMnO4酸性溶液既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 |
| B、在混有乙酸的乙酸乙酯中加入NaOH溶液可以达到除杂的目的 |
| C、丙烯的结构简式可以表示为CH3CHCH2 |
| D、CH2Cl2是纯净物说明甲烷是四面体结构而不是正方形 |
 如图,关闭活塞K,向A中充入1mol X、1mol Y,向B中充入2mol X、2mol Y,此时A、B的容积都是a L.在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+W(g);△H<0.A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L.下列说法正确的是( )
如图,关闭活塞K,向A中充入1mol X、1mol Y,向B中充入2mol X、2mol Y,此时A、B的容积都是a L.在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+W(g);△H<0.A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L.下列说法正确的是( )| A、反应速率:v(B)<v(A) |
| B、A 容器中X的转化率为80% |
| C、平衡时的压强:2p(A)=p(B) |
| D、平衡时Y的体积分数:A>B |
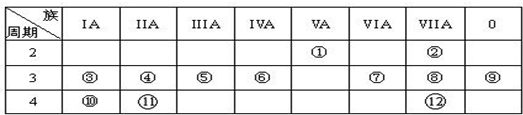
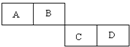 A、B、C、D四种短周期元素在周期表中的相对位置如图所示,A的单质与水蒸气反应可以制取水煤气.
A、B、C、D四种短周期元素在周期表中的相对位置如图所示,A的单质与水蒸气反应可以制取水煤气.