题目内容
根据如图所示的反应判断下列说法中错误的是( )


| A、CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量 |
| B、该反应的焓变大于零 |
| C、该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量 |
| D、由该反应可推出凡是需要加热才发生的反应均为吸热反应 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:碳酸钙受热分解是吸热反应,反应物总能量高于生成物,断键吸收的能量高于成键释放的能量,且与反应条件无关,据此分析.
解答:
解:A、反应吸热,生成物总能量高于反应物,故A正确;
B、反应吸热.焓变大于零,故B正确;
C、碳酸钙中既有离子键又有共价键,其分解时既有离子键断裂又有共价键断裂,故C正确;
D、燃烧需要加热,但都是放热反应,故D错误;
故选D.
B、反应吸热.焓变大于零,故B正确;
C、碳酸钙中既有离子键又有共价键,其分解时既有离子键断裂又有共价键断裂,故C正确;
D、燃烧需要加热,但都是放热反应,故D错误;
故选D.
点评:本题考查了吸热反应的吸热原因,从化学键和能量高低角度分析,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列表示电子转移的方法正确的是( )
A、 |
B、 |
C、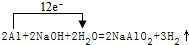 |
D、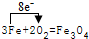 |
一定条件下,有化学反应2SO2(g)+O2(g)?2SO3(g)△H=-a kJ?mol-1,在相同条件下,要想得到2a kJ的热量,则起始加入各物质的物质的量可能是( )
| A、4mol SO2和2mol O2 |
| B、5mol SO2和3mol O2 |
| C、4mol SO2和4mol O2 |
| D、2mol SO2、1mol O2和2mol SO3 |
下列各溶液中,Na+浓度最大的是( )
| A、0.5 L 9.5mol/L的NaOH溶液 |
| B、2 L 0.4mol/L的NaN03溶液 |
| C、3L 0.3moI/L的NaCl溶液 |
| D、1 L 0.2mol/L的Na3P04溶液 |
在水溶液中的电离方程式正确的是( )
| A、NaHSO4=Na++HSO4- |
| B、NaHCO3?Na++HCO3- |
| C、MgCl2═Mg2++Cl2- |
| D、Ba(OH)2═Ba2++2OH- |
下列说法正确的是( )
| A、在101kPa下,1g物质完全燃烧所放出的热量叫该物质的热值,单位为kJ?mol-1 | ||
| B、某放热反应在其它条件不变时,加入催化剂后反应放出的热量会减少 | ||
| C、一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的 | ||
D、若一个反应的焓变△H=a kJ?mol-1,则其逆反应△H=
|