题目内容
10.碳循环与人类的生存息息相关(如图所示),下列说法不正确的是( )
| A. | CO2过度排放会导致温室效应 | |
| B. | 植物的光合作用有利于维持大气中O2和 CO2平衡 | |
| C. | 煤和石油的主要成分是有机物 | |
| D. | 碳循环过程中,碳元素均被氧化 |
分析 A.二氧化碳的排放,覆盖在地球表面,影响散热,导致地表温度升高;
B.光合作用吸收二氧化碳,释放氧气;
C.煤中主要含有碳元素,为有机物与无机物组成的混合物;石油是各种烷烃、环烷烃、芳香烃的混合物;
D.生物圈中的碳循环主要表现在绿色植物从空气中吸收二氧化碳,经光合作用转化为葡萄糖,并放出氧气,还涉及含碳的化合物之间可以相互转化,如碳酸的形成、碳酸的分解、碳酸钙和碳酸氢钙之间的转化等.
解答 解:A.二氧化碳过度排放会导致温室效应,应控制二氧化碳的排放,故A正确;
B.合作用吸收二氧化碳,释放氧气,则植物的光合作用有利于维持大气中O2和 CO2平衡,故B正确;
C.煤和石油的主要成分是有机物,故C正确;
D.生物圈中的碳循环中碳酸的形成、碳酸的分解、碳酸钙和碳酸氢钙之间的转化等都不涉及化合价的变化,碳元素不能被氧化,故D错误;
故选D.
点评 本题考查碳循环与物质的性质,为高频考点,把握发生的反应、物质的性质及环保问题为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
7.下列说法不正确的是( )
| A. | 天然油脂没有固定的熔、沸点 | |
| B. | 米饭在嘴中越咀嚼越甜的原因是淀粉水解生成甜味物质 | |
| C. | 油脂、乙醇是人体必需的营养物质 | |
| D. | 水果因含有酯类物质而具有香味 |
1.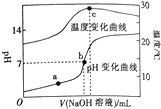 室温下,向20.00 mL 0.8mol•L-1一元酸HA溶液中滴入0.8 mol•L-1的NaOH溶液,溶液的pH和温度随加入NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )
室温下,向20.00 mL 0.8mol•L-1一元酸HA溶液中滴入0.8 mol•L-1的NaOH溶液,溶液的pH和温度随加入NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )
 室温下,向20.00 mL 0.8mol•L-1一元酸HA溶液中滴入0.8 mol•L-1的NaOH溶液,溶液的pH和温度随加入NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )
室温下,向20.00 mL 0.8mol•L-1一元酸HA溶液中滴入0.8 mol•L-1的NaOH溶液,溶液的pH和温度随加入NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )| A. | 常温下,1.0 mol•L-1HA的溶液的pH=0 | |
| B. | a、b、c三点,a点混合溶液中c(Na+)最大 | |
| C. | a、b两点的溶液中水的离子积Kw(a)=Kw(b) | |
| D. | c点时消耗NaOH溶液的体积为20.00mL |
18.a、b、c、d是原子序数依次增大的主族元素,它们的最外层电子数分别为4、1、x、7,c原子的电子层数等于x,下列说法正确的是( )
| A. | 元素a与氢元素能形成多种原子个数之比为1:1的化合物 | |
| B. | 元素b的单质不能与无水乙醇反应 | |
| C. | 元素c与元素d形成的化合物的水溶液呈碱性 | |
| D. | 元素a与元素d形成的化合物中肯定含有极性键,不可能含有非极性键 |
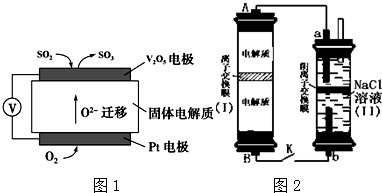
15. 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,在制备乙醛的同时能获得电能,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法不正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,在制备乙醛的同时能获得电能,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法不正确的是( )
 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,在制备乙醛的同时能获得电能,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法不正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,在制备乙醛的同时能获得电能,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法不正确的是( )| A. | 该电池可将化学能转化为电能 | |
| B. | 每有0.1 mol O2反应,则迁移0.4 mol H+ | |
| C. | 正极反应式为:CH2=CH2-2e-+2OH-═CH3CHO+H2O | |
| D. | 负极区溶液的pH减小 |
19.某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c表示止水夹).
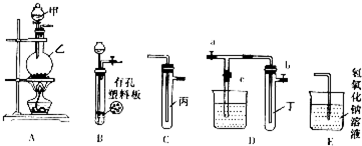
请按要求填空:
(1)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
①若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下,请将表格中实验1的现象补充:
有同学认为实验II的结论合理,请说明理由实验Ⅰ结论不合理,因为Cl2也有氧化性,此实验无法确定是Cl2还是HClO漂白;实验Ⅱ结论不合理,因为制取的氯气中含有HCl气体,HCl溶于水后能与NaHCO3粉末反应产生气泡;
②若要利用上述装置设计一个简单的实验,验证Cl-和Br-的还原性强弱,则丙中所盛装的试剂为NaBr溶液,能得到结论的实验现象为试管中溶液由无色变为橙色;
③某同学用该装置探究氯气与KI的反应,在丙中盛放有KI淀粉溶液,通入氯气,看到丙中溶液变成蓝色,继续通氯气,发现蓝色逐渐消失,检测到溶液中有含+5价元素的酸根离子,则蓝色消失过量中丙中发生反应的化学方程式是5Cl2+I2+6H2O=2HIO3+10HCl.
(2)B、D、E装置相连后,在B中盛装铜片(放在有孔塑料板上)和浓硝酸,关闭c,打开a、b,即可在试管丁中收集到NO2.
①B中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
②欲用D装置验证NO2与水的反应,在试管中收集满NO2后,使烧杯中的水进入试管丁的操作是(不可改变试管和烧杯的位置):先关闭止水夹ab,再打开止水夹c,双手紧握(或微热)试管丁使试管中气体逸出,二氧化氮与水接触后即可引发烧杯中的水倒流到试管丁中.

请按要求填空:
(1)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
①若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下,请将表格中实验1的现象补充:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有 较强的酸性 |
②若要利用上述装置设计一个简单的实验,验证Cl-和Br-的还原性强弱,则丙中所盛装的试剂为NaBr溶液,能得到结论的实验现象为试管中溶液由无色变为橙色;
③某同学用该装置探究氯气与KI的反应,在丙中盛放有KI淀粉溶液,通入氯气,看到丙中溶液变成蓝色,继续通氯气,发现蓝色逐渐消失,检测到溶液中有含+5价元素的酸根离子,则蓝色消失过量中丙中发生反应的化学方程式是5Cl2+I2+6H2O=2HIO3+10HCl.
(2)B、D、E装置相连后,在B中盛装铜片(放在有孔塑料板上)和浓硝酸,关闭c,打开a、b,即可在试管丁中收集到NO2.
①B中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
②欲用D装置验证NO2与水的反应,在试管中收集满NO2后,使烧杯中的水进入试管丁的操作是(不可改变试管和烧杯的位置):先关闭止水夹ab,再打开止水夹c,双手紧握(或微热)试管丁使试管中气体逸出,二氧化氮与水接触后即可引发烧杯中的水倒流到试管丁中.