题目内容
使相同体积的NaCl、CaCl2、AlCl3溶液中的Cl-全部沉淀,用去同浓度的AgNO3溶液的体积分别为3V、2V、V,则NaCl、CaCl2、AlCl3溶液的物质的量浓度之比为( )
| A、6:3:2 |
| B、3:2:1 |
| C、9:3:1 |
| D、1:2:3 |
考点:物质的量浓度的相关计算
专题:计算题
分析:假设硝酸银的物质的量浓度为cmol/L,完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗相同浓度的AgNO3溶液的体积分别为3V、2V、V,发生反应Ag++Cl-=AgCl↓,设NaCl、MgCl2、AlCl3溶液的浓度分别为x、y、z,溶液体积为n L,根据方程式列式计算NaCl、CaCl2、AlCl3溶液的物质的量浓度之比.
解答:
解:假设硝酸银的物质的量浓度为cmol/L,完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗相同浓度的AgNO3溶液的体积分别为3V、2V、V,
设NaCl、MgCl2、AlCl3溶液的浓度分别为xmol/L、ymol/L、zmol/L,溶液体积为n L,
根据反应Ag++Cl-=AgCl↓可得:3V×C=nL×x、2V×C=2y×n L,VC=3z×nL,
故x:y:z=
:
:
=9:3:1,
故选C.
设NaCl、MgCl2、AlCl3溶液的浓度分别为xmol/L、ymol/L、zmol/L,溶液体积为n L,
根据反应Ag++Cl-=AgCl↓可得:3V×C=nL×x、2V×C=2y×n L,VC=3z×nL,
故x:y:z=
| 3VC |
| n |
| VC |
| n |
| VC |
| 3n |
故选C.
点评:本题考查了物质的量浓度的计算、离子方程式的有关计算,题目难度不大,注意掌握物质的量浓度的概念及计算方法,明确发生的离子反应是解题关键.

练习册系列答案
相关题目
235 92 |
235 92 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
已知25℃时有关物质的电离平衡常数
下列叙述错误的是( )
| 化学式 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数 | 1.75×10-5 | 3.0×10-8 | K1=4.4×10-7 K2=4.7×10-11 |
| A、等物质的量浓度的各溶液pH关系为:pH(NaClO)>pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa) |
| B、向NaClO溶液中通入少量CO2气体反应为:ClO-+H2O+CO2=HClO+HCO3- |
| C、等物质的量浓度的HClO稀溶液与NaOH稀溶液等体积混合后溶液中:c(Na+)>c(ClO-)>c(OH-)>c(H+) |
| D、Na2CO3和NaHCO3混合液中,一定有:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
用NaOH溶液滴定盐酸时,由于滴定速率太快,当混合溶液变红时,不知NaOH是否过量,判断它是否过量的方法是( )
| A、加入5mL盐酸进行滴定 |
| B、返滴一滴待测盐酸 |
| C、重新进行滴定 |
| D、以上方法均不适用 |
下列四个数据为四个合成塔内合成氨的速度,反应速率相同的是:( )
①V(N2)=0.3mol/(L?min)
②V(NH3)=0.9mol/(L?min)
③V(H2)=0.6mol/(L?min)
④V(H2)=0.0225mol/(L?s)
①V(N2)=0.3mol/(L?min)
②V(NH3)=0.9mol/(L?min)
③V(H2)=0.6mol/(L?min)
④V(H2)=0.0225mol/(L?s)
| A、①② | B、①③ | C、③④ | D、②④ |
利用下列实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤作用的活性物质.下列说法错误的是( )
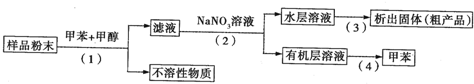

| A、步骤(1)需要过滤装置 |
| B、活性物质易溶于有机溶剂,难溶于水 |
| C、步骤(3)需要用到蒸发皿 |
| D、步骤(4)是利用物质的沸点差异进行分离的 |
下列意外事故处理的方法错误的是( )
| A、不慎将浓硫酸沾到皮肤上,立即用水冲洗,再涂上3%-5%的NaHCO3溶液 |
| B、浓碱沾到皮肤上,立即用大量的水冲洗,再涂上3%-5%的硼酸溶液 |
| C、酒精着火,应移开可燃物,用湿布或沙土盖灭 |
| D、将煤气中毒者转移到通风处抢救 |
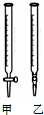 某学生用0.1000mol?L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为以下几步:
某学生用0.1000mol?L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为以下几步: