题目内容
下列推论正确的是
A.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g) ΔH=+285.8 kJ·mol-1
B.对于反应2H2O2==2H2O+O2↑,升高温度能加快O2的生成速率
C.已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2
D.在CuCl2水溶液中存在如下平衡:[Cu(H2O)4]2+(蓝)+4Cl—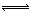 [CuCl4]2—(绿)+4H2O,若向溶液中滴加足量AgNO3溶液,可使溶液呈现绿色
[CuCl4]2—(绿)+4H2O,若向溶液中滴加足量AgNO3溶液,可使溶液呈现绿色
B
【解析】
试题分析: A、燃烧热的定义为在25℃101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,此反应为水的分解,水的状态不是液态,错误;B、升高温度能加快化学反应速率,正确;C、前者是C完全燃烧,后者是不完全燃烧,前者放出热量多,比较ΔH 时要带符号,ΔH1<ΔH2,错误;D、若向溶液中滴加足量AgNO3溶液,平衡向左移动而显蓝色,错误。
考点:ΔH的比较及平衡移动问题。

练习册系列答案
相关题目