题目内容
(7分)甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:

(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒。
②乙池中阳极的电极反应式是_________________________________________。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式____________________________________。
②甲池中碳极上电极反应式是____________________,乙池中碳极上电极反应属于____________(填“氧化反应”或“还原反应”)。
③若乙池转移0.02 mol e-后停止实验,池中溶液体积是2000 mL,则溶液混匀后的pH=________。
(1)①碳 铁 ②4OH--4e-===2H2O+O2↑ (2)①2Cl-+2H2O Cl2↑+H2↑+2OH- ②2H2O+O2+4e-===4OH- 氧化反应 ③12
Cl2↑+H2↑+2OH- ②2H2O+O2+4e-===4OH- 氧化反应 ③12
【解析】
试题分析:(1)①甲为原电池,Fe为负极,发生Fe+CuSO4═FeSO4+Cu,所以碳电极上生成红色物质Cu,乙为电解池,由电子流向可知,Fe为阴极,铜离子得到电子生成Cu,答案为:碳;铁;
②乙中阳极上氢氧根离子放电,电极反应为4OH--4e-=O2↑+2H2O,答案为:4OH--4e-=O2↑+2H2O;
(2)①电解NaCl溶液生成NaOH、H2和Cl2,离子反应为2Cl-+2H2O Cl2↑+H2↑+2OH-,答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-,答案为:2Cl-+2H2O Cl2↑+H2↑+2OH-;
Cl2↑+H2↑+2OH-;
②甲中碳为正极,氢氧根离子失去电子,电极反应为4OH--4e-=O2↑+2H2O,乙中碳为阳极,发生氧化反应;答案为:4OH--4e-=O2↑+2H2O;氧化反应;
③乙池转移0.02mole-,由2NaOH~2e-可知,n(NaOH)=0.02mol,c(NaOH)=0.02mo l /2L
=0.01mol/L,c(H+)=10-12mol/L所以pH=12。
考点:考查原电池和电解原理,分析清楚工作原理及发生的电极反应是解答的关键,注意电极的判断和电子守恒的应用

 阅读快车系列答案
阅读快车系列答案除去下列物质中的杂质,所用试剂和方法不正确的是
物质 | 杂质 | 除杂质所用试剂和方法 | |
A | KCl溶液 | I2 | CCl4,萃取 |
B | KNO3 | K2SO4 | Ba(NO3)2溶液,过滤 |
C | Cu | CuO | 盐酸,过滤 |
D | CaCO3 | CaO | 盐酸,过滤 |
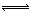 [CuCl4]2—(绿)+4H2O,若向溶液中滴加足量AgNO3溶液,可使溶液呈现绿色
[CuCl4]2—(绿)+4H2O,若向溶液中滴加足量AgNO3溶液,可使溶液呈现绿色