题目内容
14.铁粉与足量1mol/L盐酸反应,为了加快反应速率且不影响产生气体H2的量可以加入( )| A. | 少量CuSO4(s) | B. | 2mol/L的硝酸溶液 | ||
| C. | 少量铜粉 | D. | 少量CH3COONa(s) |
分析 为加快反应速率,可以升高温度或增大反应物浓度,也可以加入某些物质形成原电池,加快反应速率,但不能改变产生氢气的总量,以此解答该题.
解答 解:A.铁置换出铜,消耗铁,影响生成氢气的总量,故A错误;
B.2mol/L的硝酸溶液,硝酸与铁粉反应生成的不是氢气,故B错误;
C.少量铜粉,可以形成原电池,加快了反应速率,且不影响氢气的量,故C正确;
D.少量CH3COONa(s),生成了醋酸,降低了溶液中氢离子浓度,反应速率减小,故D错误.
故选C.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意铁和盐酸反应生成氢气而影响生成氢气的总量.

练习册系列答案
相关题目
4.下列说法中正确的是( )
| A. | 原电池的正极和电解池的阳极都是发生氧化反应 | |
| B. | 用铂做电极电解NaOH溶液时,溶质的质量不变,但浓度却随着电解的进行而增大 | |
| C. | 电解食盐水时,由于OH-离子向阳极移动,所以加酚酞时阳极附近可变红色 | |
| D. | 电解食盐水时,阴极区溶液里H+离子的浓度相对增大,使酚酞试液不变色 |
5.在我国许多地区已发生过误食亚硝酸中毒事件.人体正常的血红蛋白中含有Fe2+,若误食亚硝酸盐则导致血红蛋白中Fe2+转化为高价铁血红蛋白而中毒.服用维生素C(Vc)可解除亚硝酸盐中毒.以下说法正确的是( )
| A. | Vc将Fe3+还原为Fe2+ | B. | Vc解毒未发生氧化还原反应 | ||
| C. | 亚硝酸盐是还原剂 | D. | Vc是氧化剂 |
2.将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的是( )
①MgSO4溶液 ②Na2SO4溶液 ③饱和澄清石灰水 ④Ca(HCO3)2溶液 ⑤CuSO4溶液 ⑥饱和NaCl溶液.
①MgSO4溶液 ②Na2SO4溶液 ③饱和澄清石灰水 ④Ca(HCO3)2溶液 ⑤CuSO4溶液 ⑥饱和NaCl溶液.
| A. | ①④⑤⑥ | B. | ③④⑤⑥ | C. | ②④⑤⑥ | D. | ①③④⑥ |
9.(1)选择恰当的试剂和方法除去下列物质中的少量杂质(括号内为杂质)
(2)等物质的量的甲烷、乙烯、乙炔、苯等四种有机物分别完全燃烧,需要O2最多的是苯;等质量的上述四种物质分别完全燃烧,需要O2最多的是甲烷.
(3)目前出现的“不粘锅”、不粘油的吸油烟机等等新型厨具,其秘密就是表面有一种叫做“特 富隆”的涂层,实际上就是号称“塑料王”的聚四氟乙烯.试写出用四氟乙烯合成“特富隆”的化学方程式及其反应类型.反应方程式:nCF2=CF2→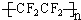 ,类型加聚反应.
,类型加聚反应.
| 除杂试剂 | 方法 | |
| C6H6 (C6H5OH) | ||
| C2H6 (C2H4) | ||
| C6H5Br (Br2) | . |
(3)目前出现的“不粘锅”、不粘油的吸油烟机等等新型厨具,其秘密就是表面有一种叫做“特 富隆”的涂层,实际上就是号称“塑料王”的聚四氟乙烯.试写出用四氟乙烯合成“特富隆”的化学方程式及其反应类型.反应方程式:nCF2=CF2→
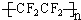 ,类型加聚反应.
,类型加聚反应.
19.下列属于氧化还原反应的是( )
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | |
| B. | Na2O+H2O=2NaOH | |
| C. | Na2CO3+H2SO4=Na2SO4+CO2↑+H2O | |
| D. | MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O |
6.在溶液中不能与Al3+大量共存的离子是( )
| A. | H+ | B. | NO- | C. | OH- | D. | Cl- |
 )是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
)是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
. )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件). $→_{催化剂△}^{H_{2}}$
$→_{催化剂△}^{H_{2}}$ $→_{光照}^{Br_{2}}$
$→_{光照}^{Br_{2}}$
 .
.
 +NaOH $→_{△}^{CaO}$R-H+Na2CO3
+NaOH $→_{△}^{CaO}$R-H+Na2CO3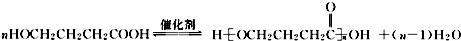 .
. .
.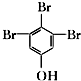 (写结构简式).
(写结构简式).