题目内容
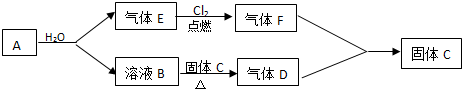
2.某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取.实验一:碘含量的测定
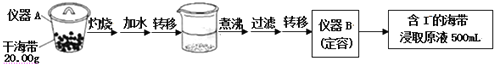
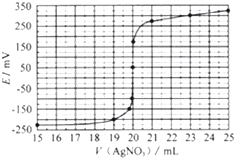
取0.0100mol/L的AgNO3标准溶液滴定100.00mL海带浸取原液,用电势滴定法测定碘的含量.测得的电动势(E)反映溶液中C(I-) 变化,用数字传感器绘制出滴定过程中曲线变化如下:
实验二:碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:
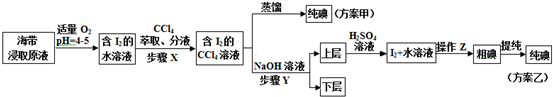
已知:3I2+6NaOH→5NaI+NaIO3+3H2O
请回答:
(1)实验一中的仪器名称:仪器A坩埚,仪器B500ml容量瓶;实验二中操作Z的名称过滤.
(2)根据表中曲线可知:此次滴定终点时用去AgNO3溶液的体积为20.00ml,计算该海带中碘的百分含量为0.635%.
(3)步骤X中,萃取后分液漏斗内观察到的现象是液体分上下两层,下层呈紫红色.
(4)下列有关步骤Y的说法,正确的是AB
A.应控制NaOH溶液的浓度和体积 B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D.NaOH溶液可以由乙醇代替
方案乙中,上层液体加硫酸发生反应的离子方程式是5I-+IO3-+6H+=3I2+3H2O.
(5)方案甲中采用蒸馏不合理,理由是碘单质易升华,会导致碘损失.
分析 (1)在仪器A中灼烧海带,该仪器为坩埚;配制溶液体积为500mL,应该选用规格为500mL的容量瓶;碘单质不溶于水,可以通过过滤操作分离出碘单质;
(2)根据图象判断滴定终点时用去AgNO3溶液的体积;根据硝酸银与碘离子的反应计算出100mL溶液中含有碘离子的物质的量,再计算出500mL溶液中含有的碘离子,最后计算出海带中碘的百分含量;
(3)碘单质易溶于有机溶剂,且四氯化碳溶液密度大于水溶液,检查判断萃取现象;
(4)A.反应3I2+6NaOH═5NaI+NaIO3+3H2O中,需要浓氢氧化钠溶液;
B.碘单质与氢氧化钠反应生成了碘化钠、碘酸钠;
C.该操作的主要目的是将碘单质转化成碘酸钠、碘化钠,便于后续分离出碘单质;
D.乙醇易溶于水和四氯化碳,仍然无法分离出碘单质.
在酸性条件下,I-和IO3-发生归中反应;
(5)从碘单质易升华角度分析.
解答 解:(1)根据仪器的构造可知,用于灼烧海带的仪器为坩埚;通过仪器B配制500mL含有碘离子的浸取液,需要使用500mL的容量瓶,步骤Z将碘单质和水分离,由于碘单质不溶于水,可通过过滤操作完成,故答案为:坩埚;500mL容量瓶;过滤;
(2)根据滴定曲线可知,当加入20mL硝酸银溶液时,电动势出现了突变,说明滴定终点时消耗了20.00mL硝酸银溶液;$\frac{127g/mol×0.001mol}{20.00g}$
20.00mL硝酸银溶液中含有硝酸银的物质的量为:0.0100mol/L×0.02L=0.0002mol,则500mL原浸出液完全反应消耗硝酸银的物质的量为:0.0002mol×$\frac{500mL}{100mL}$=0.001mol,说明20.00g该海带中含有0.001mol碘离子,所以海带中碘的百分含量为:$\frac{127g/mol×0.001mol}{20.00g}$×100%=0.635%,
故答案为:20.00;0.635%;
(3)碘单质易溶于有机溶剂,微溶于水,且四氯化碳的密度大于水溶液,所以步骤X向含有碘单质的水溶液中加入四氯化碳后,混合液会分为上下两层,下层为四氯化碳的碘溶液,则下层呈紫红色,
故答案为:液体分为上下两层,下层呈紫红色;
(4)A.发生反应3I2+6NaOH═5NaI+NaIO3+3H2O中,需要浓氢氧化钠溶液,所以应控制NaOH溶液的浓度和体积,故A正确;
B.根据反应3I2+6NaOH═5NaI+NaIO3+3H2O可知,步骤Y将碘转化成离子进入水层,故B正确;
C.该操作的主要目的是将碘单质转化成碘酸钠、碘化钠,将碘转化成离子进入水层,不是除去有机杂质,故C错误;
D.乙醇易溶于水和四氯化碳,将氢氧化钠换成乙醇,仍然无法分离出碘单质,故D错误;
在酸性条件下,I-和IO3-反应生成I2,发生反应的离子方程式为5I-+IO3-+6H+=3I2+3H2O,
故答案为:AB;5I-+IO3-+6H+→3I2+3H2O;
(5)方案甲中采用蒸馏操作,由于碘单质容易升华,会导致碘单质损失,所以甲方案不合理,故答案为:碘单质易升华,会导致碘损失.
点评 本题考查物质的分离与提纯方法的综合应用,题目难度较大,试题涉及的知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验能力,明确实验原理为解答关键,注意熟练掌握化学实验基本操作方法.

| A. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 碳酸氢铵溶液中加入过量的氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| D. | 碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| A. | 苯(甲苯):加酸性高锰酸钾溶液、再加NaOH溶液,分液 | |
| B. | 乙烷(乙烯),催化条件下通入H2 | |
| C. | 乙酸(乙醛),加入新制氢氧化铜,蒸馏 | |
| D. | 乙醛(乙酸),加入氢氧化钠溶液洗涤,蒸馏 |
| A. | CO2的电子式: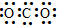 | B. | 碳原子最外层电子的轨道表示式: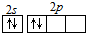 | ||
| C. | 淀粉分子的最简式:CH2O | D. | 乙烯分子的比例模型 |
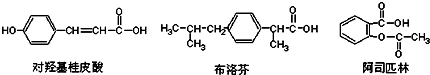
下列说法正确的是( )
| A. | 三种有机物都能发生水解反应 | |
| B. | 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 | |
| C. | 三种物质中,其中有两种互为同分异构体 | |
| D. | 三种物质在一定条件下,均可以被氧化反应 |
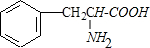 .
.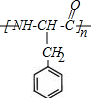 .
.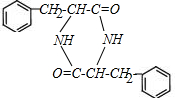 +2H2O;M与乙醇在浓硫酸、加热条件下发生反应的类型为酯化反应(取代反应).
+2H2O;M与乙醇在浓硫酸、加热条件下发生反应的类型为酯化反应(取代反应).