��Ŀ����
 ���Ŀǰ���緶Χ�ڵ���ԴΣ�����״���Ϊһ�ֽϺõĿ�������Դ�����й㷺��Ӧ��ǰ����
���Ŀǰ���緶Χ�ڵ���ԴΣ�����״���Ϊһ�ֽϺõĿ�������Դ�����й㷺��Ӧ��ǰ������1����֪�ڳ��³�ѹ�·�Ӧ���Ȼ�ѧ����ʽ��
��CO��g��+2H2��g��?CH3OH��g����H1=-90kJ?mol-1
��CO��g��+H2O��g��?CO2��g��+H2��g����H2=-41kJ?mol-1
д���ɶ�����̼�������Ʊ��״����Ȼ�ѧ����ʽ��
��2�����ݻ�ΪV L�������г���a mol CO��2a mol H2���ڴ��������·�Ӧ���ɼ״���ƽ��ʱ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
��p1
���������������������£�������a mol CO��2a mol H2���ﵽ��ƽ��ʱ��CO��ת����
��3����֪��T��ʱ��CO��g��+H2O��g��?CO2��g��+H2��g����ƽ�ⳣ��K=0.32���ڸ��¶��£���֪cʼ��CO��=1mol?L-1��cʼ��H2O��=1mol?L-1��ijʱ�̾��ⶨCO��ת����Ϊ10%����÷�Ӧ
���㣺��ѧƽ��ļ���,�ø�˹���ɽ����йط�Ӧ�ȵļ���,ת�������¶ȡ�ѹǿ�ı仯����
ר�⣺��ѧƽ��ר��
��������1�����ݸ�˹���ɺ���֪�Ȼ�ѧ����ʽ����֪������̼�������Ʊ��״����Ȼ�ѧ����ʽ���ɢ�-�ڵó���
��2����ͬ�¶��£�ͬһ�����У�����ѹǿ��ƽ��������Ӧ�����ƶ�����CO��ת���������¶Ȳ��䣬��ƽ�ⳣ�����䣻
��3������ת���ʼ�������ʵ�Ũ�ȣ���������Qc����ƽ�ⳣ����Ƚϣ����жϷ�Ӧ�Ƿ�ﵽƽ��״̬�����жϷ�Ӧ�ķ���
��2����ͬ�¶��£�ͬһ�����У�����ѹǿ��ƽ��������Ӧ�����ƶ�����CO��ת���������¶Ȳ��䣬��ƽ�ⳣ�����䣻
��3������ת���ʼ�������ʵ�Ũ�ȣ���������Qc����ƽ�ⳣ����Ƚϣ����жϷ�Ӧ�Ƿ�ﵽƽ��״̬�����жϷ�Ӧ�ķ���
���
�⣺��1����֪ʽ����CO��g��+2H2��g���TCH3OH��g����H1=-90kJ?mol-1��
��CO��g��+H2O��g���TCO2��g��+H2��g����H2=-41kJ?mol-1��
���ݸ�˹���ɽ���-�ڵã�CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H2=-49kJ?mol-1��
�ʴ�Ϊ��CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H2=-49kJ?mol-1��
��2������ͬ�¶��£�ͬһ�����У�����ѹǿ��ƽ��������Ӧ�����ƶ���CO��ת����������ͼ��֪��p1С��p2���ʴ�Ϊ��С�ڣ�
���������������������£�������a mol CO��2a mol H2���൱�ڽ�2amolCO��4amolH2����2VL�ܱ������У�����Ӧ�ﵽƽ��״̬ʱ����С�����VL������ѹǿ��ƽ��������Ӧ�����ƶ�������CO��ת��������
���ڷ�Ӧ���¶Ȳ��䣬��ƽ�ⳣ�����䣬
�ʴ�Ϊ�������䣻
��3��ijʱ�̾��ⶨCO��ת����Ϊ10%����
CO��g��+H2O��g��?CO2��g��+H2��g����
��ʼ��mol/L����1 1 0 0
ת����mol/L����0.1 0.1 0.1 0.1
ijʱ�̣�mol/L����0.9 0.9 0.1 0.1
Qc=
=0.012��0.32��
��û�дﵽƽ��״̬����Ӧ������Ӧ�����ƶ���v����v����
�ʴ�Ϊ��û�У�Qc��K������
��CO��g��+H2O��g���TCO2��g��+H2��g����H2=-41kJ?mol-1��
���ݸ�˹���ɽ���-�ڵã�CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H2=-49kJ?mol-1��
�ʴ�Ϊ��CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H2=-49kJ?mol-1��
��2������ͬ�¶��£�ͬһ�����У�����ѹǿ��ƽ��������Ӧ�����ƶ���CO��ת����������ͼ��֪��p1С��p2���ʴ�Ϊ��С�ڣ�
���������������������£�������a mol CO��2a mol H2���൱�ڽ�2amolCO��4amolH2����2VL�ܱ������У�����Ӧ�ﵽƽ��״̬ʱ����С�����VL������ѹǿ��ƽ��������Ӧ�����ƶ�������CO��ת��������
���ڷ�Ӧ���¶Ȳ��䣬��ƽ�ⳣ�����䣬
�ʴ�Ϊ�������䣻
��3��ijʱ�̾��ⶨCO��ת����Ϊ10%����
CO��g��+H2O��g��?CO2��g��+H2��g����
��ʼ��mol/L����1 1 0 0
ת����mol/L����0.1 0.1 0.1 0.1
ijʱ�̣�mol/L����0.9 0.9 0.1 0.1
Qc=
| 0.1��0.1 |
| 0.9��0.9 |
��û�дﵽƽ��״̬����Ӧ������Ӧ�����ƶ���v����v����
�ʴ�Ϊ��û�У�Qc��K������
���������⿼��ת�������¶ȡ�ѹǿ��ϵ��Ϊ��Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬��ȷ�¶ȡ�ѹǿ�Ը÷�Ӧƽ��Ӱ���ǽⱾ��ؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
�����йػ�ѧ������ȷ���ǣ�������
A��������Ϊ18����ԭ�ӽṹʾ��ͼ�� | ||
B��������Ϊ37����ԭ�ӣ�
| ||
C��Cl-�Ľṹʾ��ͼ��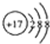 | ||
| D��NaHCO3��ˮ��Һ�еĵ��뷽��ʽ��NaHCO3=Na++H++CO32- |
��һ���¶��£�������������ֱ�ͨ����ʼ�����ͬ���ܱ�������͢��У���ͼ 1����ʹ�䷢����Ӧ��t0ʱ�������дﵽ��ѧƽ�⣬X��g����Y��g����Z��g�������ʵ����ı仯��ͼ2��ʾ���������й��ƶ���ȷ���ǣ�������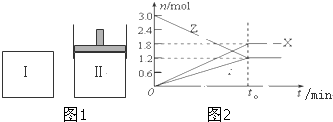

| A���÷�Ӧ�Ļ�ѧ����ʽΪ��3X+2Y?2Z |
| B�����������о��ﵽƽ��ʱ�������������V����V������������ﵽƽ������ʱ�����t0 |
| C���������о��ﵽƽ��ʱ��Z�����ʵ���������ͬ |
| D����ƽ���V��x��Ϊ1.8/t0��mol/��L?min�� |
�������µ�pH��������Ĵ��������������Һ�ֱ��ȡ���д�ʩ���й�������ȷ���ǣ�������
| A���������Ĵ����ƾ��������Һ��pH������ |
| B�������������մ�����ַ�Ӧ������Һ�в�����CO2һ���� |
| C����ˮϡ��2��������Һ��pH����С |
| D����������п��ַ�Ӧ�������в������������ʿ� |
 ����ʾ�������Ԫ�ص�ԭ���г�ȥ�������ӵ�ʣ�ಿ�֣���
����ʾ�������Ԫ�ص�ԭ���г�ȥ�������ӵ�ʣ�ಿ�֣��� ����ʾû���γɹ��ۼ����������ӣ����߱�ʾ���ۼ���
����ʾû���γɹ��ۼ����������ӣ����߱�ʾ���ۼ���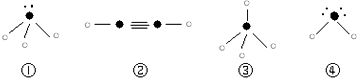
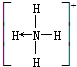 ������ʾ���õ��Ӷ���Nԭ�ӵ������ṩ���� �뻭��N4H44+�Ľṹʽ
������ʾ���õ��Ӷ���Nԭ�ӵ������ṩ���� �뻭��N4H44+�Ľṹʽ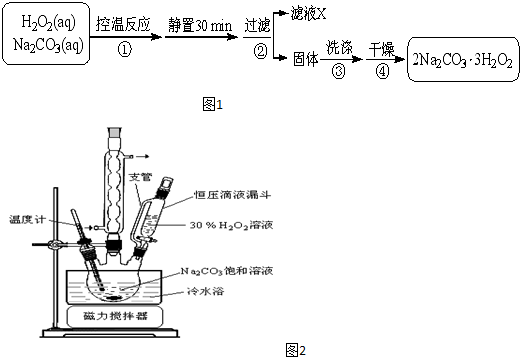
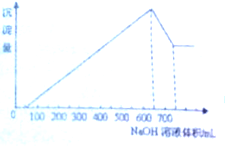 ��һ���������������������Ļ������ȫ�ܽ�100mLijŨ�ȵ������У�������������μ���1mol/L��NaOH��Һ�������������������NaOH�������ϵ��ͼ��ͼ�к�����ÿ�����ӱ�ʾ50mL����
��һ���������������������Ļ������ȫ�ܽ�100mLijŨ�ȵ������У�������������μ���1mol/L��NaOH��Һ�������������������NaOH�������ϵ��ͼ��ͼ�к�����ÿ�����ӱ�ʾ50mL����