题目内容
5.下列各组物质中,物质之间不可能实现如转化的是:( )X$\stackrel{M}{→}$Y$\stackrel{M}{→}$Z| X | Y | Z | M | |
| A | N2 | NO | NO2 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Al2O3 | NaAlO2 | Al(OH)3 | NaOH |
| D | S | SO2 | SO3 | O2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据物质的性质来判断,氮气与氧气一步反应只能生成NO,一氧化氮与氧气能生成NO2;
B、氯气与铁生成三氯化铁,三氯化铁与铁生成氯化亚铁;
C、氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠与氢氧化钠不反应;
D、硫和氧气反应生成二氧化硫,二氧化硫和氧气催化氧化生成三氧化硫.
解答 解:A、根据物质的性质来判断,氮气与氧气一步反应只能生成NO,一氧化氮与氧气能生成NO2,符合上述转化,故A不选;
B、氯气与铁生成三氯化铁,三氯化铁与铁生成氯化亚铁,符合上述转化,故B不选;
C、氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠与氢氧化钠不反应,不符合图中转化,故C选;
D、硫和氧气反应生成二氧化硫,二氧化硫和氧气催化氧化生成三氧化硫,可以实现,故D不选;
故选C.
点评 本题考查无机物的推断,侧重物质转化及物质性质的考查,明确常见物质的化学性质为解答的关键,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
15.下列有关说法正确的是( )
| A. | 分别向Na2CO3和NaHCO3溶液中逐滴加入稀盐酸至过量,产生的现象相同 | |
| B. | 分别向AlCl3溶液中逐滴加入NaOH溶液和氨水至过量,产生的现象相同 | |
| C. | 分别将FeO和Fe2O3溶于稀硝酸中,再加入KSCN溶液,溶液的颜色不同 | |
| D. | 分别向FeCl2和MgCl2溶液中,加入NaOH溶液至过量,沉淀的颜色不同 |
16.下列试剂可用带磨口玻璃塞的玻璃试剂瓶保存的是( )
| A. | 硫酸 | B. | 氢氟酸 | C. | 碳酸钠溶液 | D. | 氢氧化钠溶液 |
13.下列反应的离子方程式,正确的是( )
| A. | 碳酸钙与硝酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铁与稀硫酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | 将氨气通入盐酸中:NH3+HCl═NH4++Cl- | |
| D. | 氢氧化钡溶液中滴加稀硫酸:OH-+H+═H2O |
20.下列有关生铁和钢的说明正确的是( )
| A. | 生铁是混合物,钢是纯净物 | |
| B. | 用铁矿石来炼铁时,要加入如焦炭等氧化剂 | |
| C. | 不锈钢是铁和硅的合金,比纯铁硬度大,不易腐蚀 | |
| D. | 钢比生铁含碳量低 |
10.现有两种金属组成的混合物,把5.6g 该混合物加入到100g一定溶质质量分数的稀硫酸中,恰好完全反应,产生氢气物质的量为w.则下列说法中正确的是( )
| A. | 若混合物为Zn、Al,w不可能是0.1mol | |
| B. | 若混合物为Zn、Fe,w可能大于0.1mol | |
| C. | 若混合物为Fe、Mg,则加入的稀硫酸中溶质质量分数等于9.8% | |
| D. | 若混合物为Cu、Fe,w是0.05mol,则混合物中Fe与Cu的质量比为1:1 |
17.下列物质属于电解质的是( )
| A. | 熔融的NaOH | B. | 氨气 | C. | 蔗糖 | D. | KCl溶液 |
15.下列说法正确的是( )
| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=40.69 kJ•mol-1 | |||||||||||
| B. | Li、Be、B三种元素的第一电离能(I1)差别不大,而I2差别很大,则三种原子中最难失去第二个电子的是Be | |||||||||||
| C. | 已知:
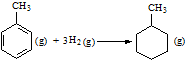 的△H为-384 kJ•mol-1 的△H为-384 kJ•mol-1 | |||||||||||
| D. | 固体NH5的所有原子的最外层均满足2个或8个电子的稳定结构,它与水反应的化学方程式为NH5+H2O═NH3•H2O+H2↑ |
