题目内容
6.现有①硫酸铜晶体,②碳酸钙固体,③纯磷酸,④硫化氢,⑤三氧化硫,⑥金属镁,⑦石墨,⑧固态苛性钾,⑨氨水,⑩熟石灰固体,其中:(1)属于强电解质的是①②⑧⑩(填序号,下同);
(2)属于弱电解质的是③④;
(3)属于非电解质的是⑤;
(4)既不是电解质,又不是非电解质的是⑥⑦⑨;
(5)能导电的是⑥⑦.
分析 在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里和熔融状态下都不导电的化合物是非电解质,完全电离的电解质是强电解质,部分电离的电解质是弱电解质,能导电的物质中含有自由移动的电子或离子.
解答 解:(1)强电解质是溶于水全部电离的电解质,①②⑧⑩是强电解质;
(2)③④是溶于水部分电离的电解质,属弱电解质;
(3)⑤属于化合物,它的水溶液虽然导电,但并不是它自身电离使溶液导电,所以是非电解质;
(4)⑥⑦都是单质,⑨是混合物,既不是电解质也不是非电解质;
(5)⑥⑦中均有能够自由移动的电子,⑨中有自由移动的离子,都能导电,其他物质都没有自由移动的电子或离子,所以不导电.
故答案为:(1)①②⑧⑩;(2)③④;(3)⑤;(4)⑥⑦⑨;(5)⑥⑦⑨.
点评 本题考查了电解质、非电解质、强弱电解质的判断,难度不大,注意这几个概念的区别.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | HNO3的摩尔质量是63g | |
| B. | 硫酸和磷酸的摩尔质量相等,都是98g/mol | |
| C. | 摩尔质量等于物质的相对原子(分子)质量 | |
| D. | 摩尔质量就是物质相对原子(分子)质量的6.02×1023倍 |
14.常温下,当水电离出的c(H+)=1×10-12mol•L-1的时候,下列离子一定不能存在的是( )
| A. | Cu2+ | B. | CO32- | C. | Na+ | D. | HSO3- |
11.下列实验操作中错误的是( )
| A. | 蒸馏操作时,冷凝水的方向应当由下往上 | |
| B. | 分液操作时,首先要打开分液漏斗的上口活塞,然后进行分液 | |
| C. | 提取碘水中的碘单质时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| D. | 萃取分液后,要得到被萃取的物质,通常还要进行蒸馏 |
18.向NaBr、NaI、Na2SO3混合液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是( )
| A. | NaCl NaBr | B. | NaCl Na2SO4 | ||
| C. | NaCl Na2SO4 I2 | D. | NaCl NaI Na2SO4 |
15.下列各组离子,在溶液中可以大量共存的是( )
| A. | H+、K+、CO32-、SO42- | B. | Na+、OH-、NH4+、Cl- | ||
| C. | Fe3+、Na+、OH-、NO3- | D. | K+、Al3+、Cl-、SO42- |

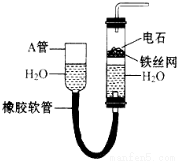 如图装置可以制取乙炔,请填空:
如图装置可以制取乙炔,请填空: