题目内容
18.用NA表示阿伏伽德罗常数的值.下列判断正确的是( )| A. | 18gH2O含有的氢分子数目为NA | |
| B. | 标准状况下,22.4LCCl4含有的分子数目为NA | |
| C. | 1L 1mol•L-1K2SO4溶液中含有的钾离子数目为NA | |
| D. | 1mol Fe与足量的稀盐酸反应,失去的电子数目为2NA |
分析 A、水中不含氢分子;
B、标况下四氯化碳为液态;
C、求出硫酸钾的物质的量,然后根据1mol硫酸钾中含2mol钾离子来分析;
D、铁和足量的盐酸反应变为+2价.
解答 解:A、水由氢原子和氧原子构成,不含氢分子,故A错误;
B、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、溶液中硫酸钾的物质的量n=CV=1mol/L×1L=1mol,而1mol硫酸钾中含2mol钾离子,故含2NA个钾离子,故C错误;
D、铁和足量的盐酸反应变为+2价,故1mol铁失去2NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)正确表示元素②在周期表中的位置第二周期第ⅣA族
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物对应的水化物是两性氢氧化物的元素是Al(填元素符号),写出它的氧化物与⑤的氢氧化物反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)⑧的单质有许多重要用途,写出其工业生产反应的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(5)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是(用离子符号表示)O2-、Na+、Mg2+.
| 列 周期 | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物对应的水化物是两性氢氧化物的元素是Al(填元素符号),写出它的氧化物与⑤的氢氧化物反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)⑧的单质有许多重要用途,写出其工业生产反应的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(5)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是(用离子符号表示)O2-、Na+、Mg2+.
3.两个容积均为1.12L的容器,在同温、同压下,一个盛满N2,另一个盛满CO气体,则两容器内气体的关系错误的是( )
| A. | 气体分子数均为3.01×1022 | B. | 密度相等 | ||
| C. | 原子数相等 | D. | 电子数相等 |
10.下列实验装置图正确的是( )
| A. |  制备及收集乙烯 | B. | 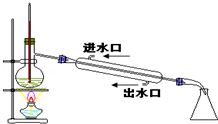 石油分馏 | ||
| C. | 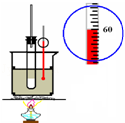 实验室制硝基苯 | D. | 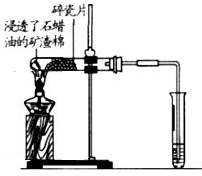 石蜡油的催化裂化 |
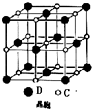 A、B、C、D 是原子序数依次增大的短周期主族元素,A 的基态原子中电 子占据三个能级,且各个能级的电子数相等;B 的一种氧化物为红棕色气体;C 的原子半径 是短周期中最大的.D 的电负性是同周期中最大的;E 是第四周期第VIII族三种元素中原子序数 最小的元素.用元素符号回答下列问题:
A、B、C、D 是原子序数依次增大的短周期主族元素,A 的基态原子中电 子占据三个能级,且各个能级的电子数相等;B 的一种氧化物为红棕色气体;C 的原子半径 是短周期中最大的.D 的电负性是同周期中最大的;E 是第四周期第VIII族三种元素中原子序数 最小的元素.用元素符号回答下列问题: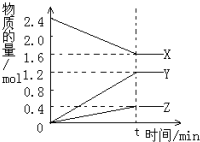 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示: