题目内容
在一真空密闭容器中盛有1mol PCl5,加热到200℃,发生反应:PCl5(g)?PCl3(g)+Cl2(g),反应达到平衡时,PCl5在混合气体中的体积分数为m%,若在相同的温度和相同的容器中,起始时加入2mol PCl5,反应达到平衡时,PCl5在混合气体中的体积分数为n%,则m 和n 关系正确性是( )
| A、m>n | B、m<n |
| C、m=n | D、无法比较 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:该反应是气体体积增大的化学反应,增大压强,平衡向逆反应方向移动,根据压强对化学平衡的影响分析.
解答:
解:根据PV=nRT知,R为常数,当V、T相同时,n越大,P越大;该反应是气体体积增大的反应,2mol>1mol,则增大压强,平衡向气体体积减小的方向移动,即逆反应方向移动,所以导致反应达到平衡时PCl5的转化率减小,PCl5的体积分数增大,故m<n.
故选B.
故选B.
点评:本题考查了外界条件对化学平衡的影响,难度较大,正确运用等效平衡是解本题的关键.

练习册系列答案
相关题目
合金在生产及科研中具有广泛的应用.下列物质不属于合金的是( )
| A、黄铜 | B、水银 | C、不锈钢 | D、硬铝 |
溶液A中加入一定量的NaF晶体后,若测得c(Na+)与c(F-)接近相等,则溶液A的pH值不可能为( )
| A、6 | B、7 | C、8 | D、9 |
如图是电解CuCl2溶液的装置,c、d为石墨电极,下列有关的判断正确的是( )
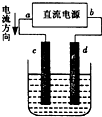

| A、电解过程中,d电极质量增加 |
| B、a为阳极、b为阴极 |
| C、a为负极、b为正极 |
| D、电解过程中,氯离子浓度基本不变 |
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法正确的是( )


| A、充电时电极b连接电源的正极 |
| B、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| C、放电时正极的电极反应式为Zn-2e-═Zn2+ |
| D、充电时左侧电解质储罐中的离子总浓度增大 |
下列说法正确的是(NA为阿伏加德罗常数)( )
| A、电解精炼铜时,当阳极上质量减少6.4g时,电路上转移的电子数目为0.2 NA |
| B、1L 1.0mol?L-1NH4Cl与2L 0.5mol?L-1NH4HSO4溶液含NH4+数目相同 |
| C、0.2mol Zn与一定量浓H2SO4恰好完全反应,生成的气体分子数必为0.2NA |
| D、将2mL0.5 mol?Lˉ1Na2SiO3溶液滴入稀盐酸中制得H4 SiO4胶体,所含胶粒数为0.001NA |