题目内容
2.下列有关金属钠在水中和在乙醇中的反应情况对比正确的是( )| A. | 钠能置换出水中所有的氢,却只能置换出乙醇里羟基中的氢 | |
| B. | 钠都要浮在水面上或乙醇液体表面 | |
| C. | 钠无论与水反应还是与乙醇反应都要放出热量 | |
| D. | 钠在乙醇中反应更剧烈,是因为乙醇分子中含有的氢原子比水分子中的多 |
分析 钠的密度比水小,比乙醇大,性质活泼,与水剧烈反应生成氢氧化钠和氢气,可与乙醇反应生成乙醇钠和氢气,与水反应较为剧烈,以此解答该题.
解答 解:A.钠和水反应生成氢氧化钠和氢气,则不能置换出水中所有的氢,故A错误;
B.钠的密度比水小,比乙醇大,在乙醇的下面,故B错误;
C.钠与水、乙醇的反应中钠都可逐渐熔化,都为放热反应,故C正确;
D.钠与水反应较为剧烈,故D错误.
故选C.
点评 本题考查钠的性质,为高频考点,侧重于钠与水、乙醇反应的对比,为高频考点,注意把握钠的性质,把握与水、乙醇反应的异同,难度不大.

练习册系列答案
相关题目
12.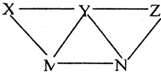 现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互转化关系,图中每条连线两端的物质可以发生化学反应.则下列推断不合理的是( )
现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互转化关系,图中每条连线两端的物质可以发生化学反应.则下列推断不合理的是( )
 现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互转化关系,图中每条连线两端的物质可以发生化学反应.则下列推断不合理的是( )
现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互转化关系,图中每条连线两端的物质可以发生化学反应.则下列推断不合理的是( )| A. | Y一定为K2CO3 | B. | X一定为H2SO4 | C. | Z可能是氯水 | D. | M可能为FeSO4 |
13.在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质.下列实验现象和结论一致且正确的是( )
| A. | 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 | |
| B. | 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在 | |
| C. | 氯水滴在PH试纸上,一段时间后将观察到试纸变红,说明H+存在 | |
| D. | 加入NaOH溶液,氯水浅黄绿色消失,说明有HClO分子存在 |
10.实验是研究化学的基础,下列图中所示的实验方法、装置和操作均正确的是( )
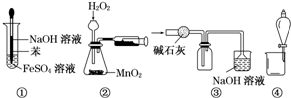

| A. | 图①可以用来制取Fe(OH)2沉淀 | |
| B. | 图②可以用来测定化学反应速率 | |
| C. | 图③可以用来收集一瓶纯净的SO2 | |
| D. | 图④可以用来分离水和乙醇的混合溶液 |
17.下列各项中表达正确的是考( )
| A. | CO2的电子式为: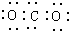 | B. | Cl2的结构式: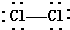 | ||
| C. | 用电子式表示NaCl的形成过程: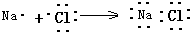 | D. | F-的结构示意图: |
7.a mol FeS与b mol FeO投入到V L、c mol•L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
(1)(a+b)×63g
(2)(a+b)×189g
(3)Vc-$\frac{(a+b)}{3}$mol
(4)Vc-$\frac{(9a+b)}{3}$mol.
(1)(a+b)×63g
(2)(a+b)×189g
(3)Vc-$\frac{(a+b)}{3}$mol
(4)Vc-$\frac{(9a+b)}{3}$mol.
| A. | (1)(3) | B. | (1)(4) | C. | (2)(3) | D. | (2)(4) |
11.下列实验能获得成功的是( )
| A. | 用溴水可鉴别苯、CCl4、苯乙烯 | |
| B. | 加浓溴水,然后过滤可除去苯中少量苯酚 | |
| C. | 苯、溴水、铁粉混合制成溴苯 | |
| D. | 鉴定溴乙烷中存在溴元素的实验操作是先加入NaOH溶液,加热后再加入AgNO3溶液 |
2.化学与生活密切相关,下列说法正确的是( )
| A. | 晶体硅可用于制造光导纤维 | B. | 氯氧化钠用来治疗胃酸过多 | ||
| C. | 铝制容器可以用来贮运稀硝酸 | D. | 乙烯用作水果的催熟剂 |