题目内容
2.化学与生活密切相关,下列说法正确的是( )| A. | 晶体硅可用于制造光导纤维 | B. | 氯氧化钠用来治疗胃酸过多 | ||
| C. | 铝制容器可以用来贮运稀硝酸 | D. | 乙烯用作水果的催熟剂 |
分析 A.光导纤维主要成分是二氧化硅;
B.氢氧化钠具有强烈腐蚀性;
C.铝与稀硝酸发生氧化还原反应,被稀硝酸腐蚀;
D.乙烯为植物生长调节剂.
解答 解:A.光导纤维主要成分是二氧化硅,不是晶体硅,故A错误;
B.氢氧化钠具有强烈腐蚀性,能够灼伤皮肤,不能用于治疗胃酸过多,故B错误;
C.铝与稀硝酸发生氧化还原反应,被稀硝酸腐蚀,所以铝制容器不可以用来贮运稀硝酸,故C错误;
D.乙烯为植物生长调节剂,可用作水果催熟剂,故D正确;
故选:D.
点评 本题考查了元素物质的性质与用途,明确硅、二氧化硅、氢氧化钠、硝酸、乙烯的性质是解题关键,注意硝酸氧化性与浓度有关,题目难度不大.

练习册系列答案
相关题目
2.下列有关金属钠在水中和在乙醇中的反应情况对比正确的是( )
| A. | 钠能置换出水中所有的氢,却只能置换出乙醇里羟基中的氢 | |
| B. | 钠都要浮在水面上或乙醇液体表面 | |
| C. | 钠无论与水反应还是与乙醇反应都要放出热量 | |
| D. | 钠在乙醇中反应更剧烈,是因为乙醇分子中含有的氢原子比水分子中的多 |
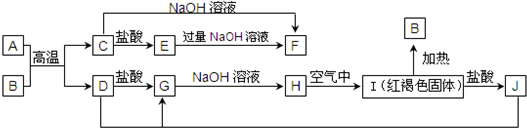
3.某溶液中有Ca2+、NH${\;}_{4}^{+}$、Mg2+、Fe2+和Al3+五种离子,若向其中加入过量的氢氧化钠溶液微热并搅拌,再加入过量盐酸,溶液中的阳离子基本不减少的是( )
| A. | NH${\;}_{4}^{+}$ | B. | Mg2+ | C. | Fe2+ | D. | Al3+ |
10.关于${\;}_{16}^{34}$S的叙述正确的是( )
| A. | 核电荷数为34 | B. | 中子数为16 | C. | 核外电子数为18 | D. | 原子序数为16 |
17.将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断不正确的是( )
| A. | 若反应中转移的电子为n mol,则n一定大于0.15 mol | |
| B. | n(NaCl):n(NaClO):n(NaClO3)可能为7:2:1 | |
| C. | 与NaOH反应的氯气一定为0.15 mol | |
| D. | n(Na+):n(Cl-) 可能为7:3 |
7.下列离子方程式书写正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 稀硫酸与氢氧化钡溶液反应:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| C. | 用氨水溶液氯化银沉淀:Ag++2NH3•H2O═[Ag(NH3)2]++2H20 | |
| D. | Fe(OH)3 溶于过量的HI溶液:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O |
14.物质的结构决定物质的性质.请回答下列涉及物质结构和性质的问题: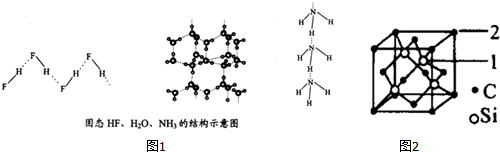
(1)第二周期中,元素的第一电离能处于B与N之间的元素有3种.
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为3d84s2
(3)乙烯酮(CH2═C═O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P═O存在下加热脱H2O得到.乙烯酮分子中碳原子杂化轨道类型是sp2和sp,1mol(C2H5O)3P═O分子中含有的σ键的数目为25NA.
(4)已知固态NH3、H2O、HF的氢键键能和结构如表:
解释H2O、HF、NH3沸点依次降低的原因单个氢键的键能是(HF)n>冰>(NH3)n,而平均每个分子含氢键数:冰中2个,(HF)n和(NH3)n只有1个,气化要克服的氢键的总键能是冰>(HF)n>(NH3)n.
(5)碳化硅的结构与金刚石类似(如图2所示),其硬度仅次于金刚石,具有较强的耐磨性能.碳化硅
晶胞结构中每个碳原子周围与其距离最近的硅原子有4个,与碳原子等距离最近的碳原子有12个.已知碳化硅晶胞边长为apm,则碳化硅的密度为$\frac{1.6×1032}{NA•a3}$g•cm3.

(1)第二周期中,元素的第一电离能处于B与N之间的元素有3种.
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为3d84s2
(3)乙烯酮(CH2═C═O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P═O存在下加热脱H2O得到.乙烯酮分子中碳原子杂化轨道类型是sp2和sp,1mol(C2H5O)3P═O分子中含有的σ键的数目为25NA.
(4)已知固态NH3、H2O、HF的氢键键能和结构如表:
| 物质 | 氢键X-H…Y | 键能KJ•mol-1 |
| (HF)n | F-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |
(5)碳化硅的结构与金刚石类似(如图2所示),其硬度仅次于金刚石,具有较强的耐磨性能.碳化硅
晶胞结构中每个碳原子周围与其距离最近的硅原子有4个,与碳原子等距离最近的碳原子有12个.已知碳化硅晶胞边长为apm,则碳化硅的密度为$\frac{1.6×1032}{NA•a3}$g•cm3.
 .
.